A、B、C、D、E是五种短周期元素。已知:它们的原子序数依次增大,A是元素周期表中原子半径最小的元素;B原子最外层电子数比其次外层电子数多2,C是E的邻族元素;D和E的原子序数之和为30,且D的族序数与周期数相等。甲、乙、 丙、丁是它们两两形成的化合物,其中甲分子中含有18个电子。
| 物质组成 | 甲 | 乙 | 丙 | 丁 |
| 化合物中各元素 原子个数比 | A和C 1:1 | B和A 1:4 | D和E 1:3 | B和E 1:4 |
⑴C的氢化物与乙相比较,稳定性强弱关系(用相应的化学式表示):_____>_ __;
⑵元素E在周期表中的位置为第 周期 族;
⑶请写出两种与乙具有相同电子数的非单核离子的化学式:_____和_____;
⑷把D的单质放到NaOH溶液中,反应的化学方程式为:______________________;
⑸写出甲的电子式:________________;
⑹有200mL MgCl2和丙的混合溶液,其中c(Mg2+)= 0.2 mol· L-1,c(Cl-)= 1.3mol·L-1,要使Mg2+全部转化为沉淀分离出来,至少需要4 mol·L-1 NaOH 溶液的体积是: __ ___。
⑴ H2O>CH4 ⑵第三周期VIIA族
⑶NH4+和OH- (其他合理答案也可)(2分)
⑷2Al+ 2NaOH+6H2O = 2Na[Al(OH)4]+3H2↑
⑸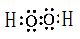 ⑹80 mL
⑹80 mL
题目分析:依据题意可以知道,A、B、C、D、E分别为H、C、O、Al、Cl,所以⑴中,C的氢化物为H2O,乙为CH4,故其稳定性强弱关系为H2O>CH4;⑵E为Cl,在周期表中的位置为第三周期VIIA族;⑶乙为CH4与乙具有相同电子数的非单核离子的化学式为NH4+和OH-;⑷D的单质为铝,其与NaOH溶液的反应为2Al+ 2NaOH+6H2O = 2Na[Al(OH)4]+3H2↑;⑸甲为过氧化氢,其电子式为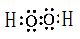 ;⑹丙为AlCl3,因为c(Mg2+)= 0.2 mol· L-1,c(Cl-)= 1.3mol·L-1,所以 MgCl2的浓度为0.2 mol· L-1,即有0.04mol,AlCl3的浓度为0.3mol· L-1,即有0.06mol,当要使Mg2+全部转化为沉淀分离出来,即要把铝离子全部转化为偏铝酸根离子,即发生
;⑹丙为AlCl3,因为c(Mg2+)= 0.2 mol· L-1,c(Cl-)= 1.3mol·L-1,所以 MgCl2的浓度为0.2 mol· L-1,即有0.04mol,AlCl3的浓度为0.3mol· L-1,即有0.06mol,当要使Mg2+全部转化为沉淀分离出来,即要把铝离子全部转化为偏铝酸根离子,即发生
Al3++4OH-=AlO2-+2H2O,消耗的 NaOH 溶液为0.24mol,将Mg2+全部转化为沉淀,即发生
Mg2++2OH-=Mg(OH)2↓,消耗的 NaOH 溶液为0.08mol,所以总共需要 NaOH 溶液0.08+0.24=0.32mol,所以0.32/4L=0.08L,即80 mL。
点评:本题考查了元素及相关化合物的性质、简单化学计算,属于高考的基础考点,本题具有一定的综合性,但是总体难度适中。

 牙面龋洞,达牙本质层,未露髓,探痛,叩痛(-),无松动,冷试验一过性敏感。
牙面龋洞,达牙本质层,未露髓,探痛,叩痛(-),无松动,冷试验一过性敏感。