乙炔(C2H2)是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙炔。
(1)CaC2中C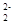 与O
与O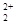 互为等电子体,等电子体结构相似,则1 个O
互为等电子体,等电子体结构相似,则1 个O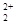 中含有的π键数目为 。
中含有的π键数目为 。
(2)将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2红棕色沉淀。Cu+基态核外电子排布式为
。
(3)乙炔与氢氰酸反应可得丙烯腈( H2C=CH—C≡N )。丙烯腈分子中碳原子轨道杂化类型是 ;分子中处于同一直线上的原子数目最多为________。
(1) 2(2分)(2)1s22s22p63s23p63d10(2分) (3)sp1杂化、sp2杂化(各2分) 3(2分)
题目分析:(1)C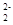 中含有碳碳三键,含有2个π键。由于C
中含有碳碳三键,含有2个π键。由于C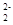 与O
与O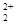 互为等电子体,等电子体结构相似,则1 个O
互为等电子体,等电子体结构相似,则1 个O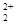 中含有的π键数目为2个。
中含有的π键数目为2个。
(2)根据构造原理可知,Cu+基态核外电子排布式为1s22s22p63s23p63d10。
(3)碳碳双键是平面型结构,碳氮三键是直线型结构,则丙烯腈分子中碳原子轨道杂化类型有sp2杂化,也有sp杂化。分子中处于同一直线上的原子数目最多为3个。
点评:该题是中等难度的试题,试题基础性强,主要是对基础知识的巩固和检验。该题的关键是明确有关概念的含义、判断依据,然后结合题意灵活运用即可。有利于培养学生的逻辑推理能力和抽象思维能力,也有助于调动学生的学习兴趣,激发学生的学习求知欲。

