一定温度范围内用氯化钠熔浸钾长石(主要成份为KAlSi3O8)可制得氯化钾,主要反应是:NaCl(l)+KAlSi3O8(s) KCl(l)+NaAlSi3O8(s)。
KCl(l)+NaAlSi3O8(s)。
(1)氯化钠的电子式是 。
(2)上述反应涉及的元素中,原子半径最大的是 。
(3)上述反应涉及的位于同一周期的几种元素中,有一种元素的最高价氧化物的水化物和其余元素的最价氧化物的水化物均能发生反应,该元素是 。
(4)某兴趣小组为研究上述反应中钾元素的熔出率(液体中钾元素的质量占样品质量的百分率)与温度的关系,进行实验(保持其它条件不变),获得如下数据:
| 时间(h) 熔出率 温度 | 1.5 | 2.5 | 3.0 | 3.5 | 4.0 | 5.0 |
| 800℃ | 0.054 | 0.091 | 0.127 | 0.149 | 0.165 | 0.183 |
| 830℃ | 0.481 | 0.575 | 0.626 | 0.669 | 0.685 | 0.687 |
| 860℃ | 0.515 | 0.624 | 0.671 | 0.690 | 0.689 | 0.690 |
| 950℃ | 0.669 | 0.714 | 0.710 | 0.714 | 0.714 | ―― |
①分析数据可以得出,氯化钠熔浸钾长石是 (填“放热”或“吸热”)反应。
②950℃时,欲提高熔出钾的速率可以采取的措施是 (填序号)。
a.充分搅拌
b.延长反应时间
c.增大反应体系的压强
d.将钾长石粉粹成更小的颗粒
(5)该方法制得KCl提纯后可用来冶炼金属钾。反应Na(l)+KCl(l) NaCl(l)+K(g)是工业上冶炼金属钾常用的方法,用平衡原理解释该方法可行的原因是 。
NaCl(l)+K(g)是工业上冶炼金属钾常用的方法,用平衡原理解释该方法可行的原因是 。
(1)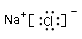 (2)K(3)Na(4)①吸热 ②a d (5)将钾分离出来,降低了产物的浓度,平衡正向移动。
(2)K(3)Na(4)①吸热 ②a d (5)将钾分离出来,降低了产物的浓度,平衡正向移动。
题目分析:(1)不难写出氯化钠的电子式是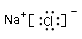 ;(2)比较离子半径:①看层,层越多,半径越大;②同层,看核,核电荷数越大,半径越小;③同层、同核看电子,电子越多半径越大,原子半径最大的是K;(3)元素钠的最高价氧化物的水化物和其余元素的最价氧化物的水化物均能发生反应;(4)温度越高,钾元素的熔出率越大,氯化钠熔浸钾长石是吸热过程;②950℃时,欲提高熔出钾的速率可以采取的措施是充分搅拌,将钾长石粉粹成更小的颗粒,增大固体的接触面积。(5)根据勒夏特列原理,可采取将钾分离出来,降低了产物的浓度,平衡正向移动。
;(2)比较离子半径:①看层,层越多,半径越大;②同层,看核,核电荷数越大,半径越小;③同层、同核看电子,电子越多半径越大,原子半径最大的是K;(3)元素钠的最高价氧化物的水化物和其余元素的最价氧化物的水化物均能发生反应;(4)温度越高,钾元素的熔出率越大,氯化钠熔浸钾长石是吸热过程;②950℃时,欲提高熔出钾的速率可以采取的措施是充分搅拌,将钾长石粉粹成更小的颗粒,增大固体的接触面积。(5)根据勒夏特列原理,可采取将钾分离出来,降低了产物的浓度,平衡正向移动。
