卤素单质可以参与很多化学反应, 如:NF3可由NH3和F2在Cu催化剂存在下反应直接得到;反应①: 2NH3+3F2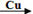 NF3+ 3NH4F
NF3+ 3NH4F
利用“化学蒸气转移法”制备TaS2晶体; 反应②:TaI4(g)+S2(g)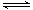 TaS2(s)+2I2(g)+Q kJ,Q>0
TaS2(s)+2I2(g)+Q kJ,Q>0
(1)反应①中:非金属性最强的元素原子核外有_________种不同运动状态的电子;该反应中的某元素的单质可作粮食保护气,则该元素最外层的电子有____________种自旋方向。
(2)反应①中:物质所属的晶体类型有________________________________;
并写出所有原子符合8电子稳定结构的化合物的电子式_______________________。
(3)反应②中:平衡常数表达式K=_____________________,若反应达到平衡后,保持其他条件不变,降低温度,重新达到平衡时 ______________。
A.平衡常数K增大
B.S2的浓度减小
C.I2的质量减小
D.V(TaI4)逆 增大(4)反应②在一定温度下进行,若反应容器的容积为2 L,3 min后达到平衡,测得蒸气的质量减少了2.45 g,则I2的平均反应速率为 _________________。
(5)某同学对反应②又进行研究,他查阅资料,发现硫单质有多种同素异形体,可表示Sx,且在一定条件下可以相互转化,他认为仅增大压强对平衡是有影响的,则TaI4的平衡转化率会____________(填增大或减小),其原因是________________________ 。
(1)9 、 2
(2)分子晶体、金属晶体、离子晶体 ;
(3)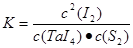 ; A B
; A B
(4)0.00333或1/300mol/(L·min)
(5)该同学认为加压对TaI4平衡转化率会减小,原因是在S2可以转化为S4或S6或S8
2TaI4(g)+S4(g)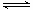 2TaS2(s)+4I2(g)加压使平衡向逆反应方向进行
2TaS2(s)+4I2(g)加压使平衡向逆反应方向进行
题目分析:
(1)在反应①中非金属性最强的元素是F,其核外电子排布是1s22s22p5.可见有9种不同运动状态的电子。在该反应中的某元素的单质可作粮食保护气,则该元素为N,其核外电子排布是1s22s22p3.在它的最外电子层有顺时针方向和逆时针方向两种不同的自旋方向。
(2)反应①中, NH3、3F2、NF3是由分子构成的分子晶体,Cu是由金属键构成的金属晶体,而NH4 F则是含有极性共价键和离子键的离子晶体。其中所有原子符合8电子稳定结构的化合物NF3的电子式是
(3)平衡常数是可逆反应达到平衡状态时各生成物浓度幂指数的乘积与个反应物浓度幂指数乘积的比。反应②中平衡常数表达式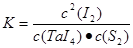 。由于反应②的正反应是气体体积增大的放热反应。所以反应达到平衡后,保持其他条件不变,降低温度,根据平衡移动原理:降低温度,化学平衡向放热反应方:向移动。对该反应来说化学平衡向正反应方向移动,所以化学平衡常数增大。正确。B.由于降低温度,平衡正向移动,所以反应物的浓度减小。正确。C. 平衡正向移动,产生更多的I2,所以c(I2)增大,I2的质量增大。错误。D. 降低温度,无论是放热反应,还是吸热反应,反应速率都减小。错误。因此正确选项为AB。
。由于反应②的正反应是气体体积增大的放热反应。所以反应达到平衡后,保持其他条件不变,降低温度,根据平衡移动原理:降低温度,化学平衡向放热反应方:向移动。对该反应来说化学平衡向正反应方向移动,所以化学平衡常数增大。正确。B.由于降低温度,平衡正向移动,所以反应物的浓度减小。正确。C. 平衡正向移动,产生更多的I2,所以c(I2)增大,I2的质量增大。错误。D. 降低温度,无论是放热反应,还是吸热反应,反应速率都减小。错误。因此正确选项为AB。
(4)n(TaS2)=" 2.45" g÷245 g/mol=0.01mol.则生成I2的物质的量为0.02mol。所以I2的平均反应速率为V=Δc÷Δt=(0.02mol÷2L)÷3min=0.00333或1/300mol/(L·min).
(5)他认为仅增大压强对平衡是有影响的,则TaI4的平衡转化率会减小,其原因是在S2可以转化为S4或S6或S8。2TaI4(g)+S4(g)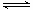 2TaS2(s)+4I2(g)加压使平衡向逆反应方向进行。
2TaS2(s)+4I2(g)加压使平衡向逆反应方向进行。
