为了维护社会秩序,保障公共安全,确保第26届世界大学生运动会的顺利进行,深圳市人民政府决定对257种化学品实施管制。氮化钠(Na3N)就是其中一种,它是科学家制备的一种重要的化合物,与水作用可产生NH3。
请根据材料完成下列问题:
(1)Na3N的电子式是 ,该化合物由 键形成。
(2)Na3N与盐酸反应生成 种盐,其电子式分别为 。
(3)Na3N与水的反应属于 反应。(填基本反应类型)
(4)比较Na3N中两种粒子的半径:r(Na+) r(N3-)(填“>”“=”或“<”)。
(1)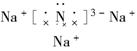 ;离子
;离子
(2)2;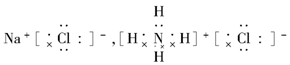
(3)复分解
(4)<
首先根据Na3N构成元素的活动性确定其所属的化合物类型,Na3N与盐酸的反应可理解为Na3N与H2O反应所得的产物再与盐酸反应。(见下图)
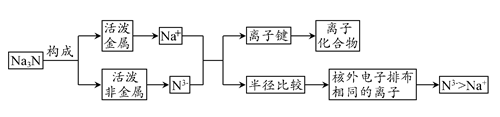
(1)钠位于第ⅠA族,是活泼金属,易失去一个电子形成Na+,N位于第ⅤA族,易得到3个电子,形成N3-,故Na+与N3-可形成离子化合物。(2)Na3N与盐酸反应时,N3-与H+结合成NH3,NH3进一步与HCl反应生成NH4Cl,Na+与Cl-形成NaCl,故有2种盐生成。(3)N3-与水的反应属于复分解反应:Na3N+3H2O=3NaOH+NH3↑。(4)Na+与N3-属于核外电子排布相同的粒子,钠的核电荷数大于氮的核电荷数,故r(Na+)<r(N3-)。
