如图为普通电池(锌锰电池)示意图,请你根据图示分析:
(1)将回收的废旧电池进行分离,可以得到的单质有(用化学式表示,
下同)______,氧化物有______,盐有______,
有机物有(写名称)______.
(2)小李同学想得到⑤中纯净干燥的二氧化锰和氯化铵溶液,并检验氯
化铵中的铵根离子.设计了如下实验步骤,请你帮他完成:
| 实验步骤 | 实验现象 | 结论或解释 |
| ①剥开干电池,取出碳棒周围的黑色粉末. | / | / |
| ②溶解、______、洗涤(填操作名称). | 得到黑色粉末和无色澄清液体 | 黑色粉末的成份为______ |
| ③对黑色粉末进行______. | / | 得到纯净的MnO2固体 |
| ④检验第②步中得到的无色澄清液体中是 否含铵根离子的方法是: ______. | ______ | 化学方程式为: ______ |
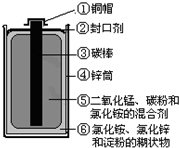
(1)单质是由同种元素组成的纯净物,碳、锌、铜等符合定义;氧化物是由两种元素组成的,且其中一种元素为氧元素的化合物,二氧化锰符合定义;盐是指由金属离子(或铵根离子)与酸根离子构成的化合物,氯化锌、氯化铵符合定义;有机物是大部分由C、H、O组成,淀粉符合定义.
故答案为:Cu、C、Zn; MnO2 ; NH4Cl、ZnCl2 ; 淀粉
(2)②碳棒周围的黑色粉末主要有二氧化锰、碳粉和氯化铵,因为氯化铵溶于水,所以可先溶解,再过滤,滤液为氯化铵溶液,滤渣是二氧化锰和碳粉.
③根据实验目的是要达到纯净干燥的二氧化锰,所以对滤渣进行灼烧,可以将碳粉变为二氧化碳除去,表面残留的氯化铵受热分解也除去了.
④根据氯化铵溶液与碱反应可以生成氨气,NH4Cl+NaOH═NaCl+H2O+NH3↑,氨气呈碱性且有刺激性气味,所以可以设计实验为取少量滤液于试管中,加入氢氧化钠溶液,然后检验生成的气体即可.
答案:
②过滤;二氧化锰和炭粉
③灼烧;④取样于试管中,加入氢氧化钠溶液并加热(把湿润的红色石蕊试纸放在试管口);强烈刺激性气味(或湿润的红色石蕊试纸变蓝色);NH4Cl+NaOH═NaCl+H2O+NH3↑
答案:
(1)Cu、C、Zn; MnO2 ; NH4Cl、ZnCl2 ; 淀粉
(2)
| 实验步骤 | 实验现象 | 结论或解释 |
| ①剥开干电池,取出碳棒周围的黑色粉末. | / | / |
| ②溶解、过滤、洗涤(填操作名称). | 得到黑色粉末和无色澄清液体 | 黑色粉末的成份为 二氧化锰和炭粉 |
| ③对黑色粉末进行 灼烧. | / | 得到纯净的MnO2固体 |
| ④检验第②步中得到的无色澄清液体中是 否含铵根离子的方法是: 取样于试管中,加入氢氧化钠溶液并加热. | 强烈刺激性气味 | 化学方程式为: NH4Cl+NaOH═NaCl+H2O+NH3↑ |
