(12分)乙酸乙酯的实验室和工业制法常采用如下反应:
CH3COOH+C2H5OH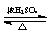 CH3COOC2H5+H2O
CH3COOC2H5+H2O
请根据要求回答下列问题:
(1)欲提高乙酸的转化率,可采取的措施有:________________、__________________等。
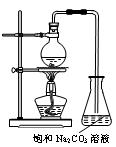
(2)若用如图(下右)所示装置来制备少量的乙酸乙酯,产率往往偏低,其原因可能为(填一点即可):____________________________________________________________________等。
(3)此反应以浓硫酸为催化剂,可能会造成(填一点即可)____________________等问题。
(4)现拟分离含乙酸、乙醇和水的乙酸乙酯产品,下图是分离操作步骤流程图。请在图中圆括号内填入适当的试剂,在方括号内填入适当的分离方法。
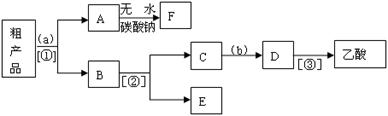
试剂a是 溶液,试剂b是 ,分离方法①是 ,分离方法②③都是 。E的结构简式为 ,在得到的A中加入无水碳酸钠粉末,振荡,目的是 。
C→D的离子方程式为 。
(1)增大乙醇的浓度 移去生成物 (2)原料来不及反应就被蒸出;温度过高,发生了副反应;冷凝效果不好,部分产物挥发了等(任填一种,合理即给分) (3)产生大量的酸性废液;造成环境污染;部分原料炭化;催化剂难以重复使用;催化效果不理想等(任填一种,合理即给分) (4)饱和碳酸钠溶液 稀硫酸 分液 蒸馏 CH3CH2OH 除去乙酸乙酯中混有的少量水 CH3COO-+H+→CH3COOH(除最后一问2分外,其余每空1分,共12分)
