下图为某实验小组制取乙酸乙酯的实验装置图,烧瓶中盛有乙醇和浓H2SO4。反应时,将乙酸从分液漏斗滴入烧瓶中即可。

①为方便研究酯化反应的过程,乙醇中的氧原子用18O进行了标记(即C2H518OH),请用氧的同位素示踪法写出乙酸与乙醇发生酯化反应的化学方程式: 。
②装置A的名称是 ,使用时要先从 口(填“a”或“b”)进水。
③实验结束后,锥形瓶中收集到乙酸乙酯、乙醇和乙酸的混合液。为了将这三者进行分离,该小组依如下流程进行了进一步的实验:
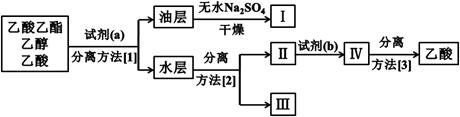
试剂(a)是 ,试剂(b)是 ,
分离方法(1)是 ,分离方法(2)是 ,分离方法(3)是 。
①CH3COOH + C2H518OH CH3CO18OC2H5 + H2O (2分)②冷凝管(1分);b(1分)③Na2CO3(也可答饱和碳酸钠溶液)(2分); H2SO4(2分,不能用盐酸和硝酸)
CH3CO18OC2H5 + H2O (2分)②冷凝管(1分);b(1分)③Na2CO3(也可答饱和碳酸钠溶液)(2分); H2SO4(2分,不能用盐酸和硝酸)
分液(2分); 蒸馏(2分); 蒸馏(2分)
题目分析:①由于在酯化反应中,羧酸提供羧基中的羟基,醇提供羟基中的氢原子,因此酯化反应的化学方程式可表示为CH3COOH + C2H518OH CH3CO18OC2H5 + H2O。
CH3CO18OC2H5 + H2O。
②根据装置的结构特点可知,A装置的名称是冷凝管。冷凝时冷却水的流向是下口进,上口出,所以使用时要先从b进水。
③由于乙酸乙酯不溶于水,而乙醇、乙酸与水互溶,因此要分离出乙酸乙酯,需要加入试剂饱和碳酸钠溶液,即a是饱和碳酸钠溶液。乙酸乙酯不溶于水,分液即可,所以分离方法(1)是分液。乙酸和碳酸钠反应生成乙酸钠,乙醇与碳酸钠不反应,但乙醇的沸点低,因此分离方法(2)是蒸馏。乙酸钠要生成盐酸,需要加入强酸。盐酸和硝酸均易挥发,所以应该用硫酸,即试剂b是硫酸。乙酸与水互溶,但乙酸与盐溶液的沸点相差较大,因此将乙酸从溶液分离出的实验操作是蒸馏。
