(14分)实验室用乙酸和正丁醇制备乙酸正丁酯。有关物质的相关数据如下表。
| 化合物 | 相对分子质量 | 密度/g·cm-3 | 沸点/℃ | 溶解度/100g水 |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
Ⅰ.乙酸正丁酯粗产品的制备
在A中加入11.5mL正丁醇和7.2mL冰醋酸,再加3~4滴浓硫酸,混合均匀,投入沸石。如图所示安装分水器、温度计及回流冷凝管,并在分水器中预先加水至略低于支管口,加热回流,反应一段时间将水逐渐分去,至反应完毕。
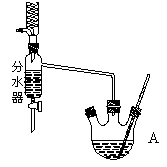
(1)仪器A中发生反应的化学方程式为____________________________。有同学拟通过某种方法鉴定所得产物中是否含有杂质,可采用 确定。
a.红外光谱法 b.1H核磁共振谱法 c.质谱法
(2)“反应中利用分水器将水分去”该操作的目的是: 。
(3)反应时加热有利于提高酯的产率,但温度过高酯的产率反而降低,其可能的原因是 。
(4)可根据 现象来判断反应完毕。
Ⅱ.乙酸正丁酯粗产品的精制
(5)将仪器A中的液体转入分液漏斗中,用分液法可分离上述有机层和水层,分液完成后,取出有机层的操作是 。
(6)再用10ml 10%Na2CO3溶液洗涤有机层,该步操作的目的是 。
(7)将干燥后的产品蒸馏收集乙酸正丁酯产品时,应将温度控制在 左右。
(1)CH3COOH+CH3CH2CH2CH2OH CH3COOCH2CH2CH2CH3+H2O(2分) a(1分)
CH3COOCH2CH2CH2CH3+H2O(2分) a(1分)
(2)将生成的产物中的水不断从反应体系中移走,促使平衡不断右移,以提高反应的转化率(2分)
(3)温度过高,丁醇与乙酸易挥发,副反应增加(2分,其他合理答案也给分)
(4)分水器中水面保持在原来高度,不再有水生成(2分)
(5)将有机层从上口倒入一个干净的烧瓶中(2分)
(6)除去产品中含有的乙酸等酸性杂质;乙酸正丁酯在饱和碳酸钠溶液中的溶解度比在水中更小,可减少乙酸正丁酯的溶解损耗(2分)
(7)126.1℃(1分)
(1)A装置是制取乙酸正丁酯的,所以方程式为
CH3COOH+CH3CH2CH2CH2OH CH3COOCH2CH2CH2CH3+H2O。红外光谱法可用于测定有机物中的官能团,所以答案选a。
CH3COOCH2CH2CH2CH3+H2O。红外光谱法可用于测定有机物中的官能团,所以答案选a。
(2)由于酯化反应是可逆反应,所以将生成的产物中的水不断从反应体系中移走,促使平衡不断右移,以提高反应的转化率。
(3)反应物酸和醇都是易挥发的,所以温度过高,丁醇与乙酸易挥发,同时副反应也增加。
(4)反应完毕时,分水器中水面将保持在原来高度,不再有水生成,据此可以判断。
(5)由于生成物酯的密度小于水的,在上层,所以将有机层从上口倒入一个干净的烧瓶中。
(6)生成的酯中含有挥发出的乙酸和丁醇,所以利用饱和碳酸钠溶液除去产品中含有的乙酸等酸性杂质;同时乙酸正丁酯在饱和碳酸钠溶液中的溶解度比在水中更小,可减少乙酸正丁酯的溶解损耗。
(7)乙酸正丁酯的沸点是126.1℃,所以蒸馏是温度应控制在126.1℃.
