X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X是元素周期表中原子半径最小的元素,X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。 请回答下列问题:
(1)Y在元素周期表中的位置为 ,ZX的电子式为 。
(2)上述元素的最高价氧化物对应的水化物酸性最强的是 (写化学式),非金属气态氢化物还原性最强的是 (写化学式)。
(3)Y、G的单质或两元素之间形成的化合物可作消毒剂的有 、 (写出其中两种物质的化学式)。
(4)X2M的标准燃烧热ΔH=-a kJ·mol-1,写出表示X2M标准燃烧热的热化学方程式: 。
(1)第二周期ⅥA族,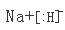
(2) HClO4,H2S
(3)O3、Cl2、ClO2(写出2种即可)
题目分析:X是元素周期表中原子半径最小的元素,X是H元素;X、Z同主族,可形成离子化合物ZX,Z是Na元素;Y、M同主族,可形成MY2、MY3两种分子。则Y、M是O、S元素;G只能是Cl元素。
(1)O在元素周期表中的位置为第二周期ⅥA族,NaH是离子化合物,所以电子式为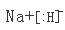
(2)上述元素的最高价氧化物对应的水化物酸性最强的也是非金属性最强的,是氯元素对应的高氯酸分子式为HClO4,非金属气态氢化物还原性最强的也是非金属性最弱的,是S对应的硫化氢,化学式为H2S;
(3)O、Cl的单质或两元素之间形成的化合物可作消毒剂的有O3、Cl2、ClO2
(4)H2S对应的稳定氧化物是液态水和气态二氧化硫,所以X2M标准燃烧热的热化学方程式为:
H2S(g)+3/2O2(g)= H2O(l)+SO2(g) ΔH=-a kJ·mol-1
