阅读理解
Thanks a Million, Dad
I was born disabled.A difficult birth, feet first, my head stuck.By my first birthday, I couldn't stand
or walk.
When I was three, the doctor told dad I had cerebral palsy (脑瘫).A loss of oxygen to my brain had
destroyed brain signals to the right side of my body.
But no son of my dad' s was going to be disabled.Every morning before breakfast and every evening
before bed, my dad placed me on the bedroom floor to exercise my right leg.The muscles were shrunk
and twisted together.Back and forth up and down, my dad pushed and pulled the muscles into shape.
But my dad' s exercise of passion didn't stop there.For my 13th birthday, he threw me a special
party.When everybody was gone, he brought me to open a large box, it was a-set of boxing gloves.
We put them on.My dad kept on beating me mercilessly.Each time I tried to get up, leather kissed
my nose, eyes and jaw.I "begged him to stop. He said he beat me to get me ready for the tough world.
That same year, I was the only kid in my neighborhood that wasn't picked for Little League. Two weeks
later.Dad started the Shedd Park Minor League, and every kid played.Dad coached us and made me
a pitcher (棒球投手).
The power of my dad' s love guaranteed I walked and more.In high school, I became a football star.
In 1997, a brain surgeon in San Jose told me I didn't t have cerebral palsy after all.He explained how
and where the doctor' s forceps (镊子) at birth had damaged my brain.
My dad never knew the whole truth since he passed away years ago.But all that counts is the bottom
line.After all his madness, on this Father' s Day, like every Father' s Day, I' m no longer disabled.
1.What caused the author' s disability?
A.A failed operation.
B.The doctor's forceps.
C.An accident in a game.
D.Shrunken and twisted muscles.
2.What do we learn from the passage?
A.The author has a talent for boxing.
B.The author achieved a lot thanks to his father' s love.
C.The author became a baseball star with the help of his father.
D.The author doesn't think his father should be so strict with him.
3.Paragraph 3 suggests that the author' s father____.
A.wouldn't give up hope easily
B.believed his son was a normal child
C.blamed the doctors for his son' s disability
D.couldn't accept the truth that his son was disabled
4.The author wrote the passage to ____.
A.remember his father
B.encourage disabled children
C.show the difficulty the disabled face
D.give advice to the parents of disabled children
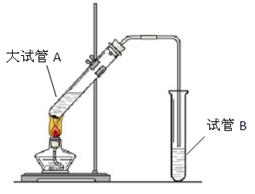
 CH3COOC2H5+H2O (2分)
CH3COOC2H5+H2O (2分) CH3COOC2H5+H2O。
CH3COOC2H5+H2O。