A~F均为元素周期表中前四周期元素,其相关信息如下表:
| 元素 | 相 关 信 息 |
| A | A的基态原子最外层电子排布式为2s22p3 |
| B | B是地壳中含量最高的元素 |
| C | C+与B的简单离子的电子层结构相同 |
| D | D的一种核素的质量数为64,中子数为35 |
| E 、F | E 、F既同周期又同族,且原子序数F比E多2 |
请回答下列问题:
(1)D的价电子的电子排布式是 ;F原子的原子结构示意图为 。
(2)A、B的第一电离能的大小顺序为 。
(3)AB3-中A原子的杂化轨道类型为_____;与A2B互为等电子体的分子的分子式为 (任写一个即可)。
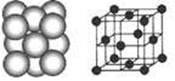
(4) D晶体的晶胞如图所示为面心立方最密堆积(在晶胞的顶点和面心均含有一个D原子)。则D的晶体中D原子的配位数为 。
(5)已知17gA的简单氢化物催化氧化生成气态水时放出QkJ的热量,请写出A的简单氢化物催化氧化的热化学反应方程式 。
(6)C2B2的电子式为____;它可与E的二氯化物溶液反应,若反应的C2B2与E的二氯化物的物质的量之比为1:2,则该反应的化学反应方程式为 。
(1)3d104s1 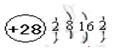
(2)N大于O
(3)sp2 CO2
(4)12
(5)4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H="-Q" kJ/mol
(5)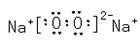 3Na2O2+6FeCl2+6H2O=6NaCl+4Fe(OH)3↓+2FeCl3
3Na2O2+6FeCl2+6H2O=6NaCl+4Fe(OH)3↓+2FeCl3
由题知,A的基态原子最外层电子排布式为2s22p3,A是N元素;B是地壳中含量最高的元素,B是O;C+与B的简单离子的电子层结构相同,C是Na;D的一种核素的质量数为64,中子数为35,D是Cu;E 、F既同周期又同族,则它们两是第四周期Ⅷ,且原子序数F比E多2,E、F分别是Fe、Ni。
(1)Cu的价电子除了4s上电子外,还包括3d上的电子;
(2)N的2p处于半充满状况,N第一电离能大于O;
(3)AB3-中N的孤电子对对数=(5+1-3×2)/2=0,即采取sp3,与N2O互为等电子体是CO2;
(4)同一个切面上的对角线顶点4个,共3个面,共12个。
