( 5 分)人类每年都要从大自然中提取大量的金属,用于满足日常生活和工农业生产
的需要。
⑴某铁厂以焦炭、赤铁矿石(主要含Fe2O3)、空气等为原料炼铁,反应过程如下:

上述工艺流程中,步骤③发生反应的化学方程式为 ,
该反应中的还原剂是 。
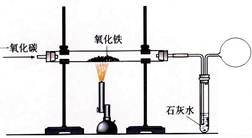
⑵实验室常用下图装置模拟炼铁反应,实验开始时,须先通 CO,再用酒精喷灯加热,这样做的目的是
。
⑶我国古代即有湿法冶金技术,古书中就有“曾青得铁则化为铜”之说,请你写出铁能从硫酸铜溶液中置换出铜单质的原因: 。
⑷在众多的金属材料中,铝及其合金一直在人类生产、生活中占据着主导地位,工业上常采用 电解氧化铝的方法来冶炼铝,该反应的化学方程式为 。
⑴ 3CO + Fe2O3 高温 2Fe + 3CO2 CO / 一氧化碳
⑵ 排净装置内的空气,防止易燃的CO发生爆炸
⑶ 在金属活动性顺序中,铁排在铜的前面 (或 铁的金属活动性强于铜)
⑷ 2Al2O3 通电 4Al + 3O2↑
题目分析:(1)步骤一是碳与氧气反应生成二氧化碳;步骤二是碳还原二氧化碳生成一氧化碳;步骤三是一氧化碳还原氧化铁:3CO + Fe2O3 高温 2Fe + 3CO2,该反应中的一氧化碳具有还原性,属还原剂;
(2)先通 CO,再用酒精喷灯加热目的是排净装置内的空气,防止易燃的CO发生爆炸;
(3)在金属活动性顺序中铁位于铜的前面,故能与铜的溶液发生置换反应;
(4)根据描述反应物是氧化铝,生成物是铝和氧气:2Al2O3 通电 4Al + 3O2↑。

