【物质结构与性质】
以氮化镓(GaN)为代表的第三代半导体材料目前已成为全球半导体研究的前沿和热点。回答下列问题:
(1)镓为元素周期表第31号元素,镓原子价层电子排布图为___________。
(2)氮所在主族中第一电离能最大的元素是________(填元素符号,下同),镓所在主族中电负性最大的元素是____________________。
(3)传统的氮化镓制备方法是采用GaCl3与NH3在一定条件下反应,该反应的化学方程式为______________。
(4)氮化镓与金刚石具有相似的晶体结构,氮化镓中氮原子与镓原子之间以____相结合,氮化镓属于_______晶体。
(5)下图是氮化镓的晶胞模型:
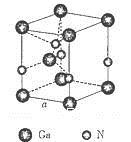
①氮化镓中镓原子的杂化方式为__________,氮原子的配位数为___________。
②氮化镓为立方晶胞,氮化镓的密度为d g/cm3。列出计算氮化镓晶胞边长a的表达式:a=_______cm。
(1)
(2)N ;B
(3)GaCl3+NH3=GaN+3HCl
(4)共价键 原子
(5)①sp2 4 ② 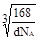
(1)镓原子序数为31,所以其核外电子排布式为:1s22s22p63s23p63d104s24p1,最外层电子为价电子,价电子排布式为:4s24p1,即4s轨道有一对自旋相反的电子,4p轨道只有一个电子,故答案为: ;
;
(2)第一电离能同主族从上到下,越来越小,N元素为该主族最上面的元素,第一电离能最大;电负性从上到下,越来越小,镓所在族最上面的元素为B;
(3)反应物为NH3和GaCl3,生成物为GaN,不难判断出另一种产物为HCl,根据原子守恒写出化学方程式,故答案为:GaCl3+NH3=GaN+3HCl;
(4)由于氮化镓与金刚石具有相似的晶体结构,所以氮化镓为原子晶体,原子之间以共价键结合在一起;
(5)①根据晶胞可以看到Ga可以相邻的三个N形成共价键,即Ga形成三条共价键,所以杂化类型为sp2杂化;观察晶胞结构发现N原子周围距离最近的Ga数目为4,即配位数为4。
②GaN晶胞中,Ga位于顶点和体心,所以含有Ga数为:8×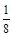 +1=2,N原子位于棱和体心,所以N数为:4×
+1=2,N原子位于棱和体心,所以N数为:4×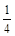 +1=2,GaN晶胞中含有两个GaN,晶胞边长为
+1=2,GaN晶胞中含有两个GaN,晶胞边长为