( 13分)下面的表格是元素周期表的一部分,其中的字母对应不同的元素。
| A | |||||||||||||||||
| M | Q | R | |||||||||||||||
| E | D | ||||||||||||||||
| G | J | ||||||||||||||||
(1)G和J形成的合金是一种贮氢材料,其晶体结构与氯化铯相同。该合金中每个G原子周围与其最近且等距的J原子有 个。该晶体属于 晶体
A .离子晶体 B . 原子晶体 C . 分子晶体 D. 金属晶体
(2)M3R2是一种直线型分子R=M=M=M=R,该分子是一种 分子(填极性或非极性)。
(3)请写出D-的电子排布式: 。
(4)M2A2也是直线型分子,1个分子中含有 个σ键。
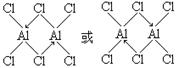
(5)化合物E2D6分子中各原子均达到了八电子稳定结构,请画出其结构式。(用元素符号表示)
(1)8 D (2)非极性 (3)1s22s22p63s23p6 (4)3
(5)
题目分析:根据元素在周期表中是位置可知:A是H;M是C;Q是N;R是O;E是Al;D是Cl;G是Ti;J是Fe。(1)Ti和Fe形成的合金是一种贮氢材料,其晶体结构与氯化铯相同。因为在氯化铯晶体中,每个Cs+离子周围与其距离相等且最近的Cl-有8个。使用该合金中每个G原子周围与其最近且等距的J原子有8个。该晶体是合金,属于金属晶体。选项为D。(2)C3O2是一种直线型分子O=C=C=C=O,。由于该分子的空间排列是对称的。所以该分子是一种非极性分子。(3)在Cl-的核外有18个电子。其电子排布式:1s22s22p63s23p6。(4)C2H2也是直线型分子,1个分子中含有3个σ键。(5)在化合物Al2Cl6分子中各原子均达到了八电子稳定结构,其结构式是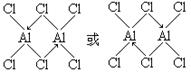 。
。
