A、B、C、D、E是五种短周期元素,原子序数依次增大。前四种的原子序数之和是E的原子序数的二倍。E的阳离子与D的阴离子都比A阳离子多2个电子层。D与四种元素中任意一种都可形成原子个数比不相同的若干种化合物。B是形成化合物种类最多的元素。请回答下列问题:
(1)写出元素符号:A________,E________。
(2)D在周期表中位于第_______周期第________族。
(3)五种元素原子半径由大到小的顺序是(用A~E字母表示)_______________。
(4)A、B、C、D可形成一种受热易分解的化合物,写出该化合物受热分解的化学方程式____________________________________________________________。
(5)A、B、D可形成A2B2D4型化合物,该化合物的名称是_____________。
(1)H,Na
(2)2,VI A
(3)E > B > C > D > A
(4)NH4HCO3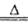 NH3↑+H2O+CO2↑
NH3↑+H2O+CO2↑
(5)乙二酸(草酸)
题目分析:(1)B是形成化合物种类最多的元素,B是C元素;D与四种元素中任意一种都可形成原子个数比不相同的若干种化合物,猜测D是O元素,则A是H元素,C是N元素,H、C、N、O的原子序数和是E的原子序数的2倍,则E是Na元素。符合Na的阳离子与O的阴离子都比H阳离子多2个电子层,说明推断正确。
(2)O在周期表中位于第2周期,第VIA;
(3)根据元素周期律中原子半径的变化规律,五种元素原子半径由大到小的顺序是E>B>C>D>A;
(4)A、B、C、D可形成一种受热易分解的化合物,该化合物是碳酸氢铵,化学方程式为NH4HCO3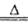 NH3↑+H2O+CO2↑;
NH3↑+H2O+CO2↑;
(5)分子式为C2H2O4的化合物是乙二酸。
