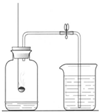
如图是某同学设计的探究空气中氧气含量的实验装置,请你协助他共同完成下列实验相关的内容.
(1)实验探究的目的是______
(2)收集的信息数据:
①空气中N2占78%,O2占21%,其它气体及杂质占1%(按体积计)
②O2可支持燃烧
③红磷、硫、木炭都可以在空气中燃烧
(3)方案设计:利用______在空气中燃烧以消耗空气中O2的实验完成(填写字母).
A.红磷 B.硫 C.木炭
(4)实验步骤:A、打开止水夹,检查装置是否漏气
B、向瓶内装少量的水,作好标记
C、等冷却至室温,打开止水夹
D、将点燃的××顺迅速伸入瓶内,并加紧橡皮塞
E、连接实验装置
其正确的操作顺序应为______(填编号)
(5)实验现象:
①红磷在集气瓶中燃烧,观察到红磷燃烧放热,______:
②打开止水夹时,观察到______.
(6)实验结论:______
(7)写出该反应的化学方程式是______.
(8)结论分析:若实验所得结论与实际结论偏离,可能的原因是(填写两点即可)
a.______ b.______
(9)启示:通过实验,我们还可知道氮气的物理性质______和化学性质______.
(1)根据题干可以知道该实验目的为探究空气中氧气的含量;
(3)红磷燃烧生成白色固体,硫燃烧生成二氧化硫气体,木炭燃烧生成二氧化碳气体,本实验的目的是测定氧气的含量,所以所选的物质不能生成气体,否则不能产生压强差,从而也就难以测定出氧气的含量,所以本实验中应该选择红磷来进行实验,故选A;
(4)实验前先连接装置,然后检查装置的气密性,在确认气密性良好的前提下向瓶内装入少量的水,作好标记,然后将点燃的××顺迅速伸入瓶内,并加紧橡皮塞,等冷却至室温,打开止水夹,即正确的顺序为:EABDC;
(5)①红磷燃烧放出热量,生成大量的白烟;
②红磷燃烧消耗了氧气而使瓶中压强减小,所以烧杯中的水会进入到瓶中约占瓶中体积的五分之一,;
(6)根据(5)中的实验现象来推断结论为:氧气约占空气体积的五分之一;
(7)红磷燃烧产生了五氧化二磷,该反应的化学方程式为:4P+5O2
2P2O5; 点燃 .
(8)该实验中应该提供足量的红磷以保证尽可能的将氧气消耗尽,同时要等装置冷却之后再打开止水夹,否则得到的结论会与实际结论有偏差;
(9)根据燃烧后水进入的体积为集气瓶体积的五分之一,而不是全部,所以可以判断氮气的物理性质为难溶于水,而过量的红磷没有完全燃烧,说明氮气不支持燃烧.
故答案为:(1)探究空气中氧气的含量;
(3)A;
(4)EABDC;
(5)①生成大量的白烟;
②烧杯中的水会进入到瓶中约占瓶中体积的五分之一,;
(6)氧气约占空气体积的五分之一;
(7)4P+5O2
2P2O5; 点燃 .
(8)红磷的量不足;没有等装置冷却就打开止水夹;
(9)难溶于水;不支持 燃烧.
