(13分)有短周期元素A、B、C、D、E、F六种短周期元素,其原子序数依次增大。其中A是周期表中原子半径最小的元素,B的核外有两个电子层,其核外电子数为两层电子数之差的三倍;A、E和D、F分别同族。D的最外层电子数等于B的原子序数。试根据以上叙述回答:
(1)写出元素符号:C____________、D____________、E_____________、F_____________;
(2)写出由A、D、E、F四种元素组成的两种盐反应的离子方程式________________________;
(3)E单质点燃时生成的淡黄色固态化合物与水反应的化学方程式:______;
(4)A与C的最低价形成的化合物为M:
① 设计简单实验验证M的浓溶液的酸碱性________________________。(写出操作、现象和结论)
②写出M催化氧化的化学方程式_________________。
(1)N O Na S (每空1分) (2) HSO3- + H+ = SO2↑+H2O(2分)
(3)2Na2O2 + 2H2O=4NaOH + O2↑(2分)
(4)①用玻璃棒蘸取该试液,滴在红色石蕊试纸上,若红色石蕊试纸变蓝,则该溶液呈碱性(3分)
②4NH3+5O2 4NO+6H2O (2分)
4NO+6H2O (2分)
题目分析:有短周期元素A、B、C、D、E、F六种短周期元素,其原子序数依次增大。其中A是周期表中原子半径最小的元素,则A是氢元素;B的核外有两个电子层,其核外电子数为两层电子数之差的三倍,因此B是碳元素;A、E和D、F分别同族,因此根据原子序数大小关系可知E是钠元素;D的最外层电子数等于B的原子序数,因此D是氧元素,则F是硫元素,C是氮元素。
(1)元素符号:C、D、E、F分别为N、O、Na、S;
(2)写出由A、D、E、F四种元素组成的两种盐分别为硫酸氢钠和亚硫酸氢钠,二者反应的离子方程式为HSO3- + H+=SO2↑+H2O;
(3)E单质点燃时生成的淡黄色固态化合物过氧化钠与水反应的化学方程式为2Na2O2 + 2H2O=4NaOH + O2↑;
(4)A与C的最低价形成的化合物为M是氨气,
①氨水显碱性,可以用红色石蕊试纸检验,即用玻璃棒蘸取该试液,滴在红色石蕊试纸上,若红色石蕊试纸变蓝,则该溶液呈碱性。
②氨气催化氧化的化学方程式为4NH3+5O2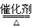 4NO+6H2O。
4NO+6H2O。