【选修3-物质结构与性质】(20分)
19-I(6分)对于钠的卤化物(NaX)和硅的卤化物(SiX4),下列叙述正确的是
A.SiX4难水解
B.SiX4是共价化合物
C.NaX易水解
D.NaX的熔点一般高于SiX4 19-Ⅱ(14分)碳元素的单质有多种形式,下图依次是C60、石墨和金刚石的结构图:
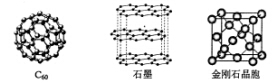
回答下列问题:
(1)金刚石、石墨、C60.碳纳米管等都是碳元素的单质形式,它们互为_____________。
(2)金刚石、石墨烯(指单层石墨)中碳原子的杂化形式分别为____、____。
(3)C60属于____晶体,石墨属于____晶体。
(4)石墨晶体中,层内C-C键的键长为142 pm,而金刚石中C-C键的键长为154 pm。其原因是金刚石中只存在C-C间的____共价键,而石墨层内的C-C间不仅存在____共价键,还有____键。
(5)金刚石晶胞含有____个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,根据硬球接触模型,则r= ______a,列式表示碳原子在晶胞中的空间占有率____(不要求计算结果)。
19-I B、D ; 19-Ⅱ(1)同素异形体(2)sp3 sp2 (3)分子 混合 (4)σ键 σ键 π键 (或大π键或p-pπ键) (5) 8 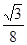
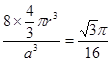
题目分析:19-I A. SiX4容易发生水解反应。错误。B. 卤素与硅但是非金属元素,所以二者结合的化合物SiX4是共价化合物。正确。C. NaX是强酸强碱盐,不发生水解反应 。错误。D. NaX是离子化合物,微粒间通过离子键结合,而SiX4则是分子晶体,分子之间通过分子间作用力结合,分子间作用力比化合价弱很多。因此NaX的熔点一般高于SiX4。正确。19-Ⅱ(1) (l)金刚石、石墨、C60、碳纳米管等都是碳元素的单质,性质不同,它们互称同素异形体。(2)在金刚石中碳原子的四个价电子与四个C原子形成四个共价键,C的杂化形式是sp3;在石墨烯(指单层石墨)中碳原子与相邻的三个C原子形成三个共价键,C的杂化形式为sp2;(3) C60是由60个C原子形成的分子,属于分子晶体。而石墨在层内原子间以共价键结合,在层间以分子间作用力结合,所以石墨属于混合晶体;(4)在金刚石中只存在C-C间的σ共价键;在石墨层内的C-C间不仅存在σ共价键,还存在π键。 (5)共价金刚石的立体网状结构金刚石晶胞,属A4型,顶点8个,相当于1个C原子,然后面心上6个,相当于3个C原子,而在其8个四面体空隙中有一半也是C原子,且在晶胞内,故还有4个C原子,加在一起,可得一个金刚石晶胞中有8个C原子。若碳原子半径为r,金刚石晶胞的边长为a,根据硬球接触模型,则正方体对角线的1/4就是C-C键的键长,即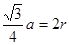 ,所以r=
,所以r=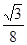 a,碳原子在晶胞中的空间占有率
a,碳原子在晶胞中的空间占有率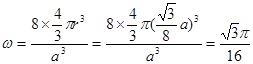 。
。
