(12分)【选做题】本题包括A、B两小题,请选定其中一小题,并在相应的答题区域内作答。若多做,则按A小题评分。
A.[物质结构与性质]
下表为元素周期表的一部分,其中的字母代表相应的元素。
| a | |||||||||||||||||
| b | c | d | |||||||||||||||
| e | f | g | |||||||||||||||
| h | I |
(2)元素c、d、e、f的第一电离能(I1)由小到大的顺序为 。(用相应元素的元素符号表示)
(3)表中所列的元素之间可以形成多种无机化合物和有机化合物,则它们形成的化合物之一——邻甲基苯甲醛的分子中碳原子轨道的杂化类型为 。
1 mol 苯甲醛分子中含有σ键的数目为 。
(4)元素d与e形成的化合物常用于制作 材料,其原因是 。
(5)表中有关元素形成的一种离子和单质d3互为等电子体,则该离子的化学式为 。
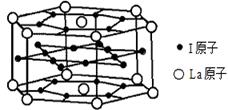
(6)元素I的合金可用来储存a的单质,该合金的晶胞结构如图所示,则此合金的化学式为 。
共12分。
(1)3d5(2分)
(2)Al<Mg<O<N(2分)
(3)sp2和sp3(2分) 14 mol或14NA(1分)
(4)耐火(1分) 晶体的晶格能较大(1分)
(5)NO2—(1分)
(6)LaNi5(2分)
题目分析:根据元素周期表可判断a~(1)根据元素周期表可判断h是Co元素,原子的外围电子的排布式为3d74s2,所以四价阳离子的外围电子排布式为3d5
(2)元素c、d、e、f分别是N、O、Mg、Al元素,N与O比,N的2p轨道是2个电子为半充满状态,所以第一电离能N>O;Mg与Al,Mg的最外层是3s轨道,有2个电子,为全充满状态,所以第一电离能Mg>Al,而电子层数越多,第一电离能越小,所以四种元素的第一电离能的大小顺序是Al<Mg<O<N;
(3)邻甲基苯甲醛的分子中苯环、醛基上的碳原子的周围有3个σ键,是sp2杂化,甲基上的碳原子周围是4个σ键,是sp3杂化;单键都是σ键,双键有1个是σ键,所以1 mol 苯甲醛分子中含有σ键的数目为14 mol或14NA;
(4)元素d与e形成的化合物是MgO,常用作耐火材料,因为MgO的晶格能较大,它的熔点高,所以被用作耐火材料;
(5)单质d3即O3,是3原子18个价电子的分子,与它互为等电子体的离子的判断,应在O元素的周围找,所以应是NO2-;
(6)元素I是Ni元素,上下底面各有6个Ni原子,侧面有 6个Ni原子,内部形成正六边形的有6个Ni原子,所以晶胞中Ni的原子个数=18×1/2+6=15;La原子位于六棱柱的顶点和上下底面的中心,所以晶胞中La原子的个数=12×1/6+2×1/2=3;所以晶胞中Ni与La的原子个数比是15:3=5:1,该晶胞的化学式为LaNi5。
