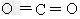短周期元素A、B、C、D中,0.5mol A元素的离子得到6.02×1023个电子被还原为中性原子,0.4g A的氧化物恰好与100ml 0.2mol/L的盐酸完全反应,A原子核内质子数目与中子数目相等,B元素原子核外第三层电子数目比第一层多1个,C-比A元素的离子多1个电子层,D元素的原子核外第二层比第一层多2个电子。回答下列问题:
(1)A、B、C、D四种元素的名称分别是_______、_______、_______、_______;
(2)C-的结构示意图为_______;D元素在周期表中的位置是__________;
(3)元素D的最简单气态氢化物的电子式为____,其分子的结构特点是具有_____结构,在一定条件下该氢化物可与单质C发生取代反应,若将等物质的量的该氢化物与单质C混合,在一定条件下充分反应后,生成物中物质的量最大的是_______(用化学式填写);
(4)工业上冶炼单质A的化学方程式为_____________________________________;
(5)工业上常用单质B冶炼难熔的金属,写出氧化铁和单质B在高温下反应的化学方程式_________________,该反应属于______反应(填“放热”或“吸热”);
(6)写出工业上用石英晶体与D的一种单质生产半导体材料的化学反应方程式_________________________;
(7)将D的单质在足量的氧气中完全燃烧,所得产物的结构式为____________。
(1)镁;铝;氯;碳
(2)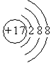 ;第二周期、ⅣA
;第二周期、ⅣA
(3)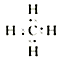 ;正四面体;HCl
;正四面体;HCl
(4)MgCl2(熔融) Mg+Cl2↑
Mg+Cl2↑
(5)Fe2O3+2Al Al2O3+3Fe;放热
Al2O3+3Fe;放热
(6) SiO2+2C ==Si+2CO↑
(7)