问题
计算题
某同学模拟工业炼铁原理,用如图所示装置进行实验。取8g氧化铁,通入足量一氧化碳,充分反应后,冷却,将玻璃管中的固体移入盛有49g硫酸溶液的烧杯中,恰好完全反应。
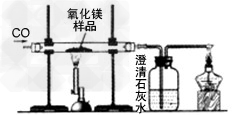
(1)该同学首先按如图所示装配好仪器,检查了气密性并装好仪器,接下来的操作是____________________________(只写一步即可)。
(2)计算硫酸溶液的溶质质量分数(要求写成计算推理过程)。
答案
(1)先通一段时间一氧化碳
(2)设8g氧化铁完全反应后生铁的质量为x。
Fe2O3+3CO 2Fe+3CO2
2Fe+3CO2
160 112
8g x

x=5.6g
设5.6g铁消耗硫酸的质量为y。
Fe+H2SO4=FeSO4+H2↑
56 98
5.6g y

y=9.8g
硫酸溶液的溶质质量分数为:(9.8g/49g)×100%=20%
答:硫酸溶液的溶质质量分数为20%。
