问题
填空题
元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了①~⑨九种元素在周期表中的位置。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ④ | ⑦ | ⑨ | |||
| 4 | ② | ⑧ |
(2)在①、②、③三种元素的氧化物对应的水化物中,碱性最强的是 (填化学式)。
(3)①、②、③三种元素按离子半径由大到小的顺序依次为 (填离子符号)。
(4)⑥元素形成的具有强氧化性的氢化物电子式是 , 该元素另一种氢化物在常温下与 ②发生反应的化学方程式为 。
答案
(1)C (2)KOH (3) 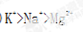 (4)
(4) 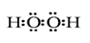
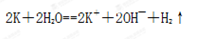
题目分析:①、②、③分别为钠,钾、铝,半径越大,碱性越强,所以碱性最强的是氢氧化钾,离子半径大小比较:电子层数越大,半径越大,电子层数相同,原子序数越大,半径越小。⑥元素为氧元素,所以形成具有强氧化性的氢化物双氧水。
