问题
填空题
(1)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关.一般地,d0或d10排布时,无颜色,d1~d9排布时,有颜色,如[Co(H2O)6]2+显粉红色.据此判断,[Mn(H2O)6]2+______颜色(填“有”“无”).
(2)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等.COCl2分子的结构式为
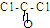
,则COCl2分子内含有______.
A.4个σ键 B.2个σ键、2个π键 C.2个σ键、1个π键 D.3个σ键、1个π键.
答案
(1)Mn2+离子的原子核外排布式为1s22s22p63s23p63d5,其d轨道上有5的电子,故[Mn(H2O)6]2+ 有颜色,
故答案为:有;
(2)COCl2分子的结构式为:
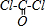
,C=O键中含有1个δ键,1个π键,则COCl2分子内含有3个σ键、1个π键,故答案为
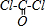
,D.
