问题
问答题
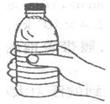
实验室中浓硫酸的商标如图所示,根据有关信息计算:(精确到0.1)
(1)该试剂瓶中硫酸溶液的质量是______g.
(2)欲配制100g溶质质量分数为19.6%的稀硫酸,需这种浓硫酸的体积是多少?
(3)取足量所配制的稀硫酸与13g锌充分反应,可制得氢气的质量是多少?

答案
(1)由密度公式可知硫酸溶液的质量为
500ml×1.84g/cm3=920g
故答案为920
(2)设需浓硫酸的体积为X
100g×19.6%=1.84g/cm3×98%X
X=10.9mL
故答案为10.9ml
(3)设可制得氢气的质量为y
Zn+H2SO4=ZnSO4+H2↑
65 2
13g y
65y=13g×2
y=0.4g
答:制的氢气的质量为0.4g