实验室可用NaBr、浓H2SO4、乙醇为原料制备少量溴乙烷:
C2H5—OH+HBr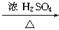 C2H5Br+H2O
C2H5Br+H2O
已知反应物的用量为:0.30 mol NaBr(s);0.25 mol C2H5OH(密度为0.80 g·cm-3);36 mL浓H2SO4(质量分数为98%,密度为1.84 g·mL-1);25 mL水。试回答下列问题。
(1)该实验应选择图中的a装置还是b装置?_____________。
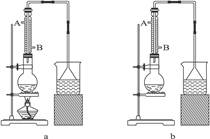
(2)反应装置中的烧瓶应选择下列哪种规格最合适( )
A.50 mL B.100 mL C.150 mL D.250 mL
(3)冷凝管中的冷凝水的流向应是 ( )
A.A进B出 B.B进A出 C.从A进或B进均可
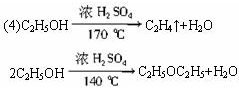
(4)可能发生的副反应为:_______________、________________、________________
(至少写出3个方程式)。
(5)实验完成后,须将烧瓶内的有机物蒸出,结果得到棕黄色的粗溴乙烷,欲得纯净溴乙烷,应采用的措施是________________。
(1)a
(2)C
(3)B
2HBr+H2SO4(浓) Br2+SO2↑+2H2O
Br2+SO2↑+2H2O
C2H5OH+2H2SO4(浓) 2C↓+2SO2↑+5H2O
2C↓+2SO2↑+5H2O
C+2H2SO4(浓) CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
(任意选取3个反应即可)
(5)将粗溴乙烷和稀NaOH(aq)的混合物放在分液漏斗中用力振荡,并不断放气,至油层无色,分液可得纯溴乙烷
(1)由题给信息,反应需要加热,所以应采用装置a。
(2)烧瓶的规格与所盛液体的体积有关,加热时烧瓶内液体的体积应介于烧瓶容积的1/3—2/3。由于:
V(C2H5OH)="0.25" mol×46 g·mol-1÷0.80 g·mL-1="14" mL
所以混合后液体的总体积约为(忽略了混合时液体体积的变化):V总≈36 mL+25 mL+14 mL="75" mL,所以150 mL的烧瓶最合适。
(3)为了防止冷凝器破裂,冷凝水应下进上出,且这样冷凝器中始终充满水,冷凝效果好。
(4)可能发生的副反应有:①C2H5OH脱水生成乙烯和乙醚,②浓H2SO4氧化HBr,③C2H5OH脱水碳化等反应。
(5)溴乙烷棕色是由于溶解了Br2,可用质量分数小于5%的稀NaOH(aq)洗涤除去,采用稀NaOH(aq)是为了防止C2H5Br的水解。
