[物质结构与性质](15分)
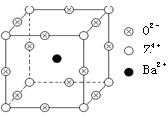
已知X、Y和Z三种元素的原子序数之和等于48。X的一种1:1型常见气态氢化物分子中既有σ键又有π键。Z是金属元素,Z的单质和化合物有广泛的用途。已知Z的核电荷数小于28,且次外层有2个未成对电子。工业上利用ZO2和碳酸钡在熔融状态下制取化合物M(M可看做一种含氧酸盐)。M有显著的“压电性能”,应用于超声波的发生装置。经X射线分析,M晶体的最小重复单位为正方体(如右图),顶点位置为Z4+所占,体心位置为Ba2+所占,所有棱心位置为O2-所占。
(1)Y在周期表中位于______________;Z4+的核外电子排布式为______________;
(2)X的该种氢化物分子构型为___________,X在该氢化物中以___________方式杂化。X和Y形成的化合物的熔点应该_____(填“高于”或 “低于”)X的该氢化物的熔点。
(3)①制备M的化学反应方程式是________________________________________;
②在M晶体中,若将Z4+置于立方体的体心,Ba2+置于立方体的顶点,则O2-处于立方体的______;
③在M晶体中,Z4+的氧配位数为________;
⑴第四周期 第ⅡA族;1s22s22p63s23p6;⑵直线形;sp;高于;⑶①TiO2+BaCO3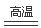 BaTiO3+CO2↑②面心;③6
BaTiO3+CO2↑②面心;③6
题目分析:根据题意可知:X是C,X的一种1:1型常见既有σ键又有π键气态氢化物分子是C2H2.Y是Ca;Z是Ti。(1)Ca在周期表中位于第四周期 第ⅡA族;Z4+的核外电子排布式为1s22s22p63s23p6;(2)X的该种氢化物分子C2H2构型为直线形;C在该氢化物中以sp方式杂化。X和Y形成的化合物CaC2是离子化合物,而C2H2的则是有分子构成的分子晶体。由于在离子化合物中离子间以离子键结合,而后者则是有分子通过分子间作用力结合的所以熔点CaC2应该高;(3)①制备M的化学反应方程式是TiO2+BaCO3 BaTiO3+CO2↑;②根据晶体结构可知,在M晶体中,含Ba:1;含有Ti:8×1/8=1;含有O:12×1/4=3.所以该晶体的化学式是BaTiO3。在BaTiO3晶体中,若将Ti4+置于立方体的体心,Ba2+置于立方体的顶点,则O2-只能处于立方体的面心,③在M晶体中,由晶胞可知,每个Ti4+周围有6个O2-,所以Ti4+的氧配位数为为6,所以Ti4+的氧配位数为6个。
BaTiO3+CO2↑;②根据晶体结构可知,在M晶体中,含Ba:1;含有Ti:8×1/8=1;含有O:12×1/4=3.所以该晶体的化学式是BaTiO3。在BaTiO3晶体中,若将Ti4+置于立方体的体心,Ba2+置于立方体的顶点,则O2-只能处于立方体的面心,③在M晶体中,由晶胞可知,每个Ti4+周围有6个O2-,所以Ti4+的氧配位数为为6,所以Ti4+的氧配位数为6个。
