问题
问答题
(3分)16g Fe2O3与184g稀H2SO4恰好完全反应,求所得Fe2(SO4)3溶液的溶质质量分数?
答案
(3分)解:设反应生成的Fe2(SO4)3的质量为x
Fe2O3+3H2SO4===Fe2(SO4)3+3H2O (1分)
160 400
16g x
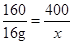
x=40g (1分)
溶质的质量分数为: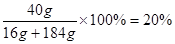 (1分)
(1分)
答:所得溶液的溶质质量分数为20%。
本题考查的是根据化学反应方程式的计算,有关溶质质量分数的简单计算。首先根据反应物,生成物和反应条件正确书写方程式,再根据方程式中Fe2O3和Fe2(SO4)3的质量比求出Fe2(SO4)3的质量,由公式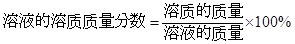 ,就可以求出所得Fe2(SO4)3溶液的溶质质量分数。
,就可以求出所得Fe2(SO4)3溶液的溶质质量分数。
解:设反应生成的Fe2(SO4)3的质量为x
Fe2O3+3H2SO4===Fe2(SO4)3+3H2O
160 400
16g x
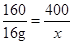
解得 x=40g
溶质的质量分数为: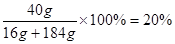
答:所得溶液的溶质质量分数为20%。
