图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图: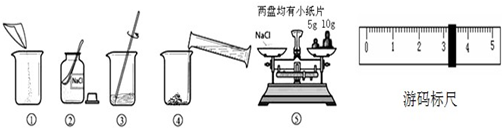
(1)用上图表示的序号表示配制溶液的正确操作顺序______.
(2)图②中,有一种塑料仪器,其名称是______.
(3)称量NaCl时,天平平衡后的状态如图⑤所示,游码标尺示数见右图,则称取的NaCl质量为______.
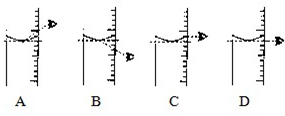
(4)根据计算需要量取水的体积是______(水的密度为1g/mL).量取读数时,如图视线角度正确的是______.(选填字母标号)
(5)称量NaCl质量完毕放回砝码时,发现有一个砝码缺损了一个小角,若其他操作步骤正确,则所配溶液的溶质质量分数______(填“大于”、“小于”或“等于”)10%.
(6)若测得溶液的质量分数大于10%,请你分析可能的原因(写两条):______;______.
(1)称量食盐的质量首先打开广口瓶塞,倒放在桌面上,将取得的食盐放在天平的左盘,然后将称得的食盐放到烧杯中,再将量取的水倒入烧杯中,用玻璃棒搅拌使之溶解,故正确的顺序为②⑤①④③;
(2)图②中的塑料仪器为药匙;
(3)食盐的质量=砝码+游码,据图可知,砝码的读数是15g,游码的读数是3.2g,故食盐的质量=15g+3.2g=18.2g;
(4)氯化钠溶液的质量=18.2g÷10%=182g,所以水的质量=182g-18.2g=163.8g,所以量取水的体积是163.8ml,量取读数时,视线应与液体凹液面的最低处保持水平,故选D;
(5)砝码缺少一角则称量的食盐的质量减小,溶质减少,则溶液变稀,溶质质量分数变小;
(6)配制溶液后,测得溶液的质量分数大于10%,导致质量分数偏大的原因:溶质氯化钠量偏大或溶剂水的量偏小;
故答:故答案为:(1)②⑤①④③;
(2)药匙;
(3)18.2g;
(4)163.8ml;D;
(5)小于;
(6)称量NaCl的实际质量比计算质量大;加入水的实际量比计算量小;
