(2011年湖南株洲,31题) 某化学兴趣小组,在一次查阅“关于如何治疗人体胃酸过多"的资料后,决定利用实验室相关仪器(高温消毒)自制小苏打水(NaHCO3水溶液),用来缓解胃酸过多的症状。具体配制步骤(经医生建议)如下:
第一步:准确称量8.4g食品级小苏打粉末;第二步:将第一步所称粉末配成100g溶液;
第三步:将第二步所得溶液取出10g,再加水配制成100g溶液即得到治疗胃酸过多的小苏打水(密度为1.0g/mL)。
请回答下列问题:
(1)第—步用到的主要仪器是 ;第二步使用的玻璃仪器有 (至少写两种);
(2)第三步配制所得的小苏打水中NaHCO3的质量分数是 ;
(3)胃酸过多者在医生的指导下,每次喝50mL第三步配制所得的小苏打水,一天两次,则一天可反应掉胃液中的HCl g。
(1)托盘天平(天平);玻璃棒、烧杯、量筒; (2) 0.84% (3)0.365
析:(1)根据溶液的配制选择所用仪器;
(2)根据溶质的质量分数计算公式进行解答;
(3)根据小苏打与稀盐酸反应的化学方程式解答.
解答:解:(1)称量要用到托盘天平,配制溶液还要用到烧杯,加速溶解的玻璃棒,量取一定量液体的量筒;
故答案为:托盘天平; 玻璃棒、烧杯、量筒(任写2种即可);
(2)第二步所得溶液溶质质量分数是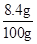 ×100%=8.4%,小苏打为10g×8.4%=0.84g,溶液是100g,溶质的质量分数
×100%=8.4%,小苏打为10g×8.4%=0.84g,溶液是100g,溶质的质量分数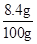 ×100%=0.84%;
×100%=0.84%;
故答案为:0.84%;
(3)每天摄入的小苏打的质量50mL×2×1.0g/mL×0.84%=0.84g.
是设可反应掉胃液中的HCl 的质量为X.
NaHCO3+HCl=NaCl+H2O+CO2↑
84 36.5
0.84g X
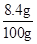 =
=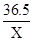
X=0.365g
故答案为:0.365g.
