(15分)乙醇、乙酸都是有机化工重要的基础原料。
(1).空气中,乙醇蒸气能使红热铜丝保持红热,该反应的化学方程式为 。
(2).浓硫酸催化下,乙酸和乙醇生成乙酸乙酯
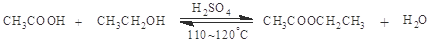
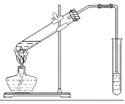
某化学兴趣小组的同学用以下装置进行该酯化反应的探究实验:
①要向大试管中加2mL浓硫酸、3mL乙醇、2mL乙酸,其具体操作是 。
②小试管中装的是浓Na2CO3溶液,导气管不插入液面下是为了防止 。
③相关物质的部分性质:
| 乙醇 | 乙酸 | 乙酸乙酯 | |
| 沸点 | 78.0℃ | 117.9℃ | 77.5℃ |
| 水溶性 | 易溶 | 易溶 | 难溶 |
⑤分离时,乙酸乙酯应该从仪器 (填“下口放” 或“上口倒出”)。
⑥兴趣小组多次试验后,测出乙醇与乙酸用量和最后得到的乙酸乙酯生成量如下表:
| 实验序号 | 乙醇(mL) | 乙酸(mL) | 乙酸乙酯(mL) |
| a | 2 | 2 | 1.33 |
| b | 3 | 2 | 1.57 |
| c | 4 | 2 | X |
| d | 5 | 2 | 1.76 |
| e | 2 | 3 | 1.55 |
⑴2CH3CH2OH + O2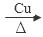 2CH3CHO + 2H2O
2CH3CHO + 2H2O
(2)①大试管中加入3mL乙醇,然后边振荡试管边加入2mL浓硫酸和2mL乙酸。②倒吸;
③不能,乙酸乙酯在乙醇、乙酸和水的混合溶液中溶解度比较大。④分液漏斗 ;上口倒出
⑤1.57-1.76mL; 探究乙酸用量对乙酸乙酯产量的影响。
题目分析:(1)空气中,乙醇蒸气能使红热铜丝保持红热,该反应的化学方程式为2CH3CH2OH + O2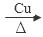 2CH3CHO + 2H2O; (2)①要向大试管中加2mL浓硫酸、3mL乙醇、2mL乙酸,其具体操作是先向大试管中加入3mL乙醇,然后边振荡试管边加入2mL浓硫酸,待溶液冷却后再加入2mL乙酸。②小试管中装的是浓Na2CO3溶液,其作用是吸收挥发的乙醇蒸气,反应消耗蒸发出来的乙酸,减少其气味的产生;降低乙酸乙酯的溶解度,以便于混合物的分离提纯。导气管不插入液面下是为了防止倒吸现象的发生。③不能用水替代小试管中的Na2CO3溶液,是因为乙酸乙酯在乙醇、乙酸和水的混合溶液中溶解度比较大。④分离小试管中互不相溶的两层液体混合物的方法是分液,使用的仪器是分液漏斗。⑤在分离时,由于乙酸乙酯的密度比水小,在上层,使用应该从仪器上口倒出;⑥根据表中数据变化规律可知:表中数据X的范围是1.57-1.76mL;实验a与实验e中乙醇的用量相同,而乙酸用量不同,乙醇这两组使用探究的目的是探究乙酸用量对乙酸乙酯产量的影响。
2CH3CHO + 2H2O; (2)①要向大试管中加2mL浓硫酸、3mL乙醇、2mL乙酸,其具体操作是先向大试管中加入3mL乙醇,然后边振荡试管边加入2mL浓硫酸,待溶液冷却后再加入2mL乙酸。②小试管中装的是浓Na2CO3溶液,其作用是吸收挥发的乙醇蒸气,反应消耗蒸发出来的乙酸,减少其气味的产生;降低乙酸乙酯的溶解度,以便于混合物的分离提纯。导气管不插入液面下是为了防止倒吸现象的发生。③不能用水替代小试管中的Na2CO3溶液,是因为乙酸乙酯在乙醇、乙酸和水的混合溶液中溶解度比较大。④分离小试管中互不相溶的两层液体混合物的方法是分液,使用的仪器是分液漏斗。⑤在分离时,由于乙酸乙酯的密度比水小,在上层,使用应该从仪器上口倒出;⑥根据表中数据变化规律可知:表中数据X的范围是1.57-1.76mL;实验a与实验e中乙醇的用量相同,而乙酸用量不同,乙醇这两组使用探究的目的是探究乙酸用量对乙酸乙酯产量的影响。
