如图所示为LC振荡电路中电容器的极板带电荷量随时间变化曲线,下列判断中正确的是( ).

A.在b和d时刻,电路中电流最大
B.在a→b时间内,电场能转变为磁场能
C.a和c时刻,磁场能为零
D.在O →a和c→d时间内,电容器被充电
ABC
a和c时刻是充电结束时刻,此时刻电场能最大,磁场能最小为零,C正确;b和d时刻是放电结束时刻,此时刻电路中电流最大,A正确;a→b是放电过程,电场能转化为磁场能,B正确;O →a是充电过程,而c→d是放电过程,D错误.
如图所示为LC振荡电路中电容器的极板带电荷量随时间变化曲线,下列判断中正确的是( ).

A.在b和d时刻,电路中电流最大
B.在a→b时间内,电场能转变为磁场能
C.a和c时刻,磁场能为零
D.在O →a和c→d时间内,电容器被充电
ABC
a和c时刻是充电结束时刻,此时刻电场能最大,磁场能最小为零,C正确;b和d时刻是放电结束时刻,此时刻电路中电流最大,A正确;a→b是放电过程,电场能转化为磁场能,B正确;O →a是充电过程,而c→d是放电过程,D错误.
TiO2俗称钛白粉,用途广泛,现正广泛开发,将来有机会成为新工业。工业上利用TiO2制备金属钛的流程如下。
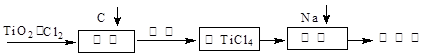
已知:I.
Ti(s)+O2(g)=TiO2(s) △H=-946 kJ·mol-1
2C(s)+O2(g)=2CO(g) △H=-221 kJ·mol-1
Ti(s)+2Cl2(g)=TiCl4(g) △H=-815 kJ·mol-1
II.某温度下各物质的沸点如下:
| 物质 | TiCl4 | FeCl3 | SiCl4 | AlCl3 |
| 沸点/℃ | 136 | 310 | 56.5 | 180 |
回答下列问题:
(1)在氯化工序中发生反应:TiO2(s)+2Cl2(g)+2C(s)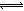 TiCl4(g)+2CO (g) 。试计算其反应的△H= kJ•mol-1;反应的平衡常数表达式K= ,在下图中作出TiCl4达到平衡后百分含量随温度的变化趋势图。
TiCl4(g)+2CO (g) 。试计算其反应的△H= kJ•mol-1;反应的平衡常数表达式K= ,在下图中作出TiCl4达到平衡后百分含量随温度的变化趋势图。

(2)氯化过程中带入的副产物有FeCl3、SiCl4和AlCl3,可用 方法获得较纯净的TiCl4。
(3)TiO2与Cl2反应:TiO2(s)+2Cl2(g)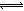 TiCl4(l)+O2(g)△H=+151kJ•mol-1。该反应在高温条件下但难以发生,但加入碳后反应能顺利进行,试解析上述原因
TiCl4(l)+O2(g)△H=+151kJ•mol-1。该反应在高温条件下但难以发生,但加入碳后反应能顺利进行,试解析上述原因
(4)还原工序要在惰性气体的气氛中进行的理由是_______________________。
(5)制取Ti的新工艺是用二氧化钛作阴极,以石墨为阳极,以CaCl2熔盐做电解质(在熔融状态下能传导O2-),电解而得到Ti,该工艺具有操作简单,成本低,无污染等优点,写出电解制备金属钛时阴极的电极反应式: 。