液化石油气是家庭常用燃料,主要成分是丙烷和丁烷。
| 性质 物质 | 熔点/ ℃ | 沸点/ ℃ | 燃烧反应 |
| 丙烷 | —189.7 | —42.1 | 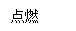
|
| 丁烷 | —138.4 | —0.5 | 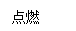
|
由上表资料分析,丙烷和丁烷的物理性质是:常温常压下呈________态(填“气”、“液”或“固”);化学性质是:具有 ________ 性。
液化石油气燃烧需要大量的氧气。根据化学方程式计算:59g丁烷充分燃烧所需要的氧气的质量。
(3)已知含碳气体的含氢量越高,相同条件下充分燃烧时产生CO2就越少。比较甲烷、丙烷和丁烷分子中氢的质量分数,看出最洁净的燃料是______________(填化学式)。
气体燃料具有价廉、使用方便等优点,但使用时应特别注意安全问题。
①若灶具上的风板调节不好,空气供应不足,燃烧不充分,其后果是_____________________、
_____________________________________。
②烧水或做饭时,人不要远离灶具。如果火焰熄灭而又没有及时关闭燃气灶,可燃性气体会在厨房里扩散,遇明火会发生_______________的危险。
气体 可燃性 211.6g CH4 产生有害气体CO, 使人中毒、浪费燃料; 爆炸
分析:(1)根据题目所给的信息进行解答;
(2)利用化学方程式根据丁烷的质量可以求出氧气的质量;
(3)根据甲烷、丙烷和丁烷分子的化学式可以比较氢的质量分数;
(4)根据含碳气体不完全燃烧的产物进行解答,以及可燃性气体不纯会发生爆炸进行解答.
解答:解:(1)丙烷和丁烷的沸点为-42.1℃和-0.5℃,所以常温常压下呈气态,因为丙烷和丁烷都能和氧气反应生成二氧化碳和水,所以它们的化学性质是都具有可燃性;
(2)设59g丁烷充分燃烧所需要的氧气的质量为x.
2C4H10+13O2 8CO2+10H2O
8CO2+10H2O
116 416
59g x
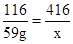
x=211.6g
答:59g丁烷充分燃烧所需要的氧气的质量为211.6g.
(3)可以将甲烷、丙烷、丁烷的化学式CH4、C3H8、C4H10都转化为C12H48、C12H32、C12H30,当碳原子个数相同,氢原子最多的氢的质量分数也要越大,所以甲烷是最洁净的燃料;
(4)①含碳气体的燃料由于空气供应不足,燃烧不充分,会生成一氧化碳,而一氧化碳有毒,所以若灶具上的风板调节不好,空气供应不足,燃烧不充分,其后果是煤气中毒以及浪费燃料;②由于可燃性气体不纯遇到明火会发生爆炸.
故答案为:(1)气、可燃;(2)211.6g;(3)CH4;(4)产生有害气体CO,使人中毒、浪费燃料;爆炸.

 C3H8+5O2 3CO2+4H2O
C3H8+5O2 3CO2+4H2O 2C4H10+13O2 8CO2+10H2O
2C4H10+13O2 8CO2+10H2O