问题
选择题
取3.2g某物质R在4.8g氧气中恰好完全燃烧,生成3.6g水和4.4g二氧化碳,关于R的下列说法中,正确的是
A.R中含有C、H、O三种元素
B.R中C与H的质量比为1:4
C.R属于无机化合物
D.R只含有C、H两种元素,是一种清洁燃料
答案
答案:A
分析:根据物质的质量和化学式可以计算出生成物中各种元素的质量,再根据质量守恒定律可以确定R的组成、元素质量比、类别和用途.
解:3.6g水中氢元素的质量为3.6g×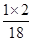 ×100%=0.4g
×100%=0.4g
3.6g水中氧元素的质量为3.6g×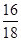 ×100%=3.2g
×100%=3.2g
4.4g二氧化碳中碳元素的质量为4.4g×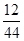 ×100%=1.2g
×100%=1.2g
4.4g二氧化碳中氧元素的质量为4.4g×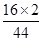 ×100%=3.2g
×100%=3.2g
生成物中氧元素的质量为3.2g+3.2g=6.4g>4.8g,6.4g-4.8g=1.6g.
根据质量守恒定律中元素质量守恒的特点可知:R中含有1.6g氧元素.
根据质量守恒定律中元素质量守恒的特点还可知:R中含有0.4g氢元素和1.2g碳元素.
所以:
R中含有碳、氢、氧三种元素,因此选项A正确.
R中碳与氢的质量比为1.2g:0.4g=3:1,因此选项B错误.
R中含有碳元素,符合有机物的概念,因此属于有机物,不属于无机物,因此选项C错误.
R中含有碳、氢、氧三种元素,不是只含碳、氢元素,因此选项D错误.
故选A.
