有A、B、C、D、E五种微粒(原子或离子),已知:
A原子核外M电子层上有2个电子;
B原子得到2个电子后,其电子层结构与Ne相同;
C离子带有一个单位的正电荷,核电荷数为11;
D离子核外有18个电子,质子数比电子数少一个;
E微粒不带电,其质量数为1.
试回答下列问题:
(1)依次写出A、B、C、D、E各微粒的符号
A______、B______、C______、D______、E______;
(2)C、D所属元素组成的化合物是______化合物(填共价或离子),用电子式表示其形成过程______.
A原子核外M电子层上有2个电子,则处于ⅡA,A为Mg原子;B原子得到2个电子后,其电子层结构与Ne相同,B的质子数为10-2=8,B为氧原子;C离子带有一个单位的正电荷,核电荷数为11,则C离子为Na+;D离子核外有18个电子,质子数比电子数少一个,质子数为18-1=17,D离子为Cl-;E微粒不带电,其质量数为1,不含中子,则E为H原子,
(1)由上述分析可知,A为Mg、B为O、C为Na+、D为Cl-、E为H原子,故答案为:Mg;O;Na+;Cl-;H;
(2)C、D所属元素组成的化合物是NaCl,属于离子化合物,用电子式表示其形成过程: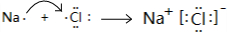 ,
,
故答案为:离子;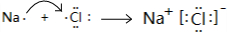 .
.
