问题
多选题
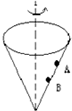
在光滑的圆锥形漏斗的内壁,有两个质量相等的小球A、B,它们分别紧贴漏斗,在不同水平面上做匀速圆周运动,如图所示,则下列说法正确的是( )
A.小球A的速率大于小球B的速率
B.小球A的速率小于小球B的速率
C.小球A对漏斗壁的压力大于小球B对漏斗壁的压力
D.小球A的转动周期大于小球B 的转动周期
答案
对A、B两球进行受力分析,两球均只受重力和漏斗给的支持力FN.如图所示
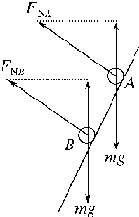
对A球由牛顿第二定律:
FNAsinα=mg----------------------①
FNAcosα=m
=mωA2rA-----------------------②vA2 rA
对B球由牛顿第二定律:
FNBsinα=mg----------------------③
FNBcosα=m
=mωB2rB-------------------------④vB2 rB
由两球质量相等可得FNA=FNB,所以C错误.
由②④可知,两球所受向心力相等.
m
=mvA2 rA
,因为rA>rB,所以vA>vB,故A正确,B错误.vB2 rB
mωA2rA=mωB2rB,因为rA>rB,所以ωA<ωB,故又因为ω=
,所以TA>TB,故D正确.2π T
故选AD.
