某同学学习了氨气之后,对其很感兴趣,上网查阅资料获得如下信息:
氨气(NH3)是一种无色有刺激性气味的气体,密度比空气小,易溶于水,不可燃.氨气能与氧化铜在加热条件下反应生成铜、空气中含量最多的气体和一种液体.
于是他进行了如下实验:
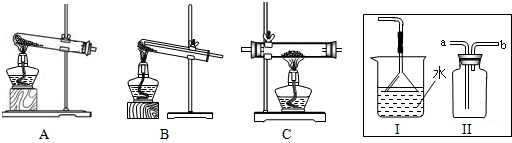
(1)请写出氨气与氧化铜反应的化学方程式:______;
(2)氨气与氧化铜的反应最好在上述装置______(填序号)中完成;该装置后通常还需接装置Ⅰ,原因是:______;
(3)进行该实验时,操作顺序合理的是______(填字母);
a.先通氨气,后点燃酒精灯 b.先点燃酒精灯,后通氨气 c.a、b都可以
(4)实验室若用装置Ⅱ收集氨气,气体应当从管口______(选填“a”或“b”)进入.
(1)由题意可知,氨气与氧化铜在加热条件下反应生成铜、空气中含量最多的气体和一种液体.空气中含量最多的气体是氮气,由质量守恒定律可知,一种液体是水,反应的方程式是:2NH3+3CuO
3Cu+N2+3H2O; △ .
(2)由于氨气与氧化铜在加热条件下反应,氨气有刺激性气味会污染空气且易溶于水.为了防止氨气溢出进入空气,应选用装置C来完成,尾气应处理,可用装置Ⅰ来处理;
(3)由于氨气与氧化铜在加热条件下反应,不会发生爆炸,先通氨气,后点燃酒精灯或先点燃酒精灯,后通氨气都可以;
(4)由于氨气的密度小于空气的密度,应选择b为进气口.
故答为:(1)2NH3+3CuO
3Cu+N2+3H2O; (2)C、氨气有刺激性气味会污染空气且易溶于水;(3)c;(4)b. △ .
