[物质结构与性质]
氧是地壳中含量最多的元素
(1)氧元素基态原子核外未成对电子数为______个.
(2)H2O分子内O-H键、分子间的范德华力和氢键从强到弱依次为______.
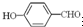
沸点比
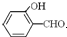
高,原因是______.
(3)H+可与H2O形成H3O+,H3O+中O原子采用______杂化.H3O+中H-O-H键角比H2O中H-O-H键角大,原因是______.
(4)CaO与NaCl的晶胞同为面心立方结构,已知CaO的密度为ag•cm-3,NA表示阿伏家的罗常数,则CaO晶胞的体积为______
cm3.
(1)氧元素基态原子核外电子排布式为1s22s22p4,4个电子在三个轨道中排布,故未成对电子数为2个,故答案为:2;
(2)共价键的键能大于氢键的作用力,氢键的作用力还大于范德华力,故H2O分子内的O-H键、分子间的范德华力和氢键从强到弱依次为O-H键、氢键、分子间的范德华力;含分子间氢键的物质的沸点大于分子内氢键物质的沸点,因此原因是前者易形成分子间氢键,后者易形成分子内氢键.
故答案为:O-H键、氢键、范德华力;
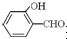
形成分子内氢键,而
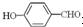
形成分子间氢键,分子间氢键使分子间作用力增大;
(3)H3O+价层电子对模型为四面体,氧原子采取sp3杂化.
H2O中O原子有两对孤对电子,H3O+中O原子有一对孤对电子,因为孤电子对间的排斥力>孤电子对与成键电子对间的排斥力>成键电子对间的排斥力,导致H3O+中H-O-H键角比H2O中H-O-H键角大.
故答案为:sp3;H2O中O原子有两对孤对电子,H3O+中O原子有一对孤对电子,排斥力较小
(4)1个“CaO”的质量为
=56g/mol NA/mol
g,而用均摊法算出一个晶胞含有4个“CaO”,即一个晶胞质量为56 NA
g×4=56 NA
g,又有ρ=224 NA
,则V=m V
,m ρ
V=
g÷ag/cm3=224 NA
cm3,则CaO晶胞体积为 224 aNA
cm3.224 aNA
故答案为:
.224 aNA
