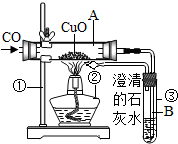
在学习一氧化碳化学性质时,关于一氧化碳还原氧化铜的实验,老师让同学们设计实验装置.三个组的同学设计了如下甲、乙、丙三套实验装置,请根据下列要求回答有关问题:
|
|
|
| 甲 | 乙 | 丙 |
(2)实验开始时,要先通一会儿一氧化碳然后再加热,其目的是______;
实验结束时,为了防止生成的铜被空气氧化,要注意先______.
(3)根据要求填表:
| 装置 | 实验现象 | 简 答 |
| A装置 | ______ | 反应的化学方程式:______ 氧化剂是______ |
| B装置 | ______ | 反应的化学方程式:______ |
(5)将符合上述装置组合设计意图的标号填写在空格上______.
①说明一氧化碳具有还原性; ②既说明一氧化碳具有可燃性;又充分地利用了能源;
③说明一氧化碳得氧后的产物是二氧化碳; ④有效地防止了一氧化碳的扩散到空气中.
(6)实验中当4g氧化铜完全被还原时,请计算参加该反应的一氧化碳气体的物质的量.(写出计算过程)
(1)仪器名称为:铁架台、酒精灯
(2)一氧化碳具有可燃性,加热一氧化碳与空气混合气体可能发生爆炸,实验开始时,要先通一会儿一氧化碳然后再加热
目有的是排尽玻璃管中的空气,防止一氧化碳与空气混合后发生爆炸.实验结束时要先熄灭酒精灯停止加热,继续通一氧化碳到试管冷却.防止生成的铜又被氧化成氧化铜;
(3)一氧化碳还原氧化铜生成铜和二氧化碳,故看到的现象为:黑色粉末逐渐变红;化学方程式为 CO+CuO
CO2+Cu,氧化铜失去氧被还原. △ .
二氧化碳与氢氧化钙反应生成难溶于水的碳酸钙,故澄清石灰水变浑浊,化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O
(4)丙装置将剩余的一氧化碳作为燃料给氧化铜加热,这样变废为宝;充分利用能源;更能有效利用能源.
(5)上述实验可以说明说明一氧化碳具有还原性;说明一氧化碳具有可燃性;又充分地利用了能源;
一氧化碳得氧后的产物是二氧化碳; 有效地防止了一氧化碳的扩散到空气中.
(6)根据化学方程式已知氧化铜的质量,求参加反应的一氧化碳的物质的量.
故答案为:(1)铁架台、酒精灯
(2)排尽玻璃管中的空气,防止一氧化碳与空气混合后发生爆炸.
先熄灭酒精灯停止加热,继续通一氧化碳到试管冷却.
(3)黑色粉末逐渐变红; CO+CuO
CO2+Cu,氧化铜或CuO; △ .
澄清石灰水变浑浊; Ca(OH)2+CO2=CaCO3↓+H2O
(4)变废为宝;充分利用能源;更能有效利用能源(合理即给分).
(5)①②③④
(6)设:至少需要一氧化碳的质量为x
CO+CuO
CO2+Cu, △ .
28 80
x 4g
=28 x
x=1.4g80 4g
所以一氧化碳的物质的量为
=0.05mol1.4g 28g/mol