碘缺乏症遍及全球,多发生于山区。南美的安第斯山区、欧洲的阿尔卑斯山区和亚洲的喜马拉雅山区是高发病地区。我国云南、河南等10余省的山区发病率也较高。据估计我国患者大约有1000万人。为控制该病的发生,较为有效的方法是食用含碘食盐,我国政府以国家标准的方式规定在食盐中添加碘酸钾(KIO3)。据此回答下列问题:
(1)碘是合成下列哪种激素的主要原料之一
A.胰岛素 B.甲状腺激素 C.生长激素 D.雄性激素
(2)长期生活在缺碘山区,又得不到碘盐的供应,易患
A.甲状腺亢进 B.佝偻病 C.地方性甲状腺肿 D.糖尿病
(3)可用盐酸酸化的碘化钾和淀粉检验食盐中的碘酸钾。反应的化学方程式为 。氧化产物与还原产物的物质的量之比为 。能观察到的明显现象是 。
(4)已知KIO3可用电解方法制得。总反应化学方程式为:KI+3H2O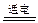 KIO3+3H2↑。在某温度下.若以12 A的电流强度电解KI溶液10 min.理论上可得标况下氢气___________L。
KIO3+3H2↑。在某温度下.若以12 A的电流强度电解KI溶液10 min.理论上可得标况下氢气___________L。
(1)B (2)C
(3)5KI+KIO3+6HCl===6KCl+3I2+3H2O 5∶1 溶液变蓝
(4)0.837
此题重点考查了一些卫生保健的常识及与其有关的化学知识。碘是合成甲状腺激素的主要原料之一,缺碘易患地方性甲状腺肿。这一病症可用食含碘食盐的方法来预防,这些内容属于卫生保健的常识性知识。但检验食盐中是否含碘及如何制取碘盐中所需的KIO3,则需用化学知识来解决。在酸性条件下,IO3-可氧化I-生成单质碘,碘遇淀粉变为蓝色。反应的化学方程式为:5KI+KIO3+6HCl=6KCl+3I2+3H2O。I2既是氧化产物,又是还原产物,其物质的量之比为5∶1。
本题的第(4)小题是利用电学知识解决化学问题。
依据Q=It和1个电子的电量为1.60×10-19C
n(e-)=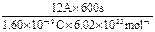 =7.475×10-2 mol
=7.475×10-2 mol
V(H2)=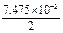 mol×22.4 L·mol-1=0.837 L
mol×22.4 L·mol-1=0.837 L
