联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。回答下列问题:
(1)联氨分子的电子式为(),其中氮的化合价为()。
(2)实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为()。
(3)①2O2(g)+N2(g)==N2O4(l) ΔH1
②N2(g)+2H2(g)==N2H4(l) ΔH2
③O2(g)+2H2(g)==2H2O(g) ΔH3
④2N2H4(l)+N2O4(l)==3N2(g)+4H2O(g)ΔH4=-1048.9kJ•mol-1
上述反应热效应之间的关系式为ΔH4=(),联氨和N2O4可作为火箭推进剂的主要原因为()。
(4)联氨为二元弱碱,在水中的电离方式与氨相似。联氨第一步电离反应的平衡常数值为()(已知:N2H4+H+N2H5+的K=8.7×107;Kw=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为()。
(5)联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象是()。联氨可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O2()kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是()。
参考答案:
(1)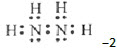
(2)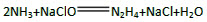
(3)2ΔH3−2ΔH2−ΔH1反应放热量大、产生大量气体
(4)8.7×10−7;N2H6(HSO4)2
(5)固体逐渐变黑,并有气泡产生1N2H4的用量少,不产生其他杂质(还原产物为N2和H2O,而Na2SO3产生Na2SO4)
