(1)(6分)化学用语是学习化学的基础,请用化学用语填空。
①两个氮分子 ;②人体中含量最多的常量元素 ;③+2价的镁元素 ;
④三个硫酸根离子 ;⑤氦气 ;⑥氧元素质量分数最高的氧化物 。
(2)(6分)在化学反应中,物质所含元素的化合价发生变化的反应就是氧化还原反应。
例如:2Na+C12=2NaCl,反应前后Na、C1元素的化合价发生了变化,该反应是氧化还原反应。
①含有高价态元素的化合物,在反应前后元素的化合价降低,通常具有氧化性。如:氯化铁溶液能和单质铜反应生成氯化铜和另一种铁的氯化物。该反应的化学方程式可表示为 ,该反应中,
元素的化合价发生了变化,反应物中表现出氧化性的物质是 ;②向上述反应后的溶液中加入过量的锌粉充分反应后过滤,则滤纸上一定有的固体是 ,滤液中的溶质是 。反思与评价:有人认为复分解反应一定不是氧化还原反应,请你也从化合价角度解释原因 。
(3)(3分)用“O”和“●”分别代表两种不同元素的原子,这两种元素组成的物质在一定条件下能发生以下反应,反应前后的微观模拟图如下:

①该反应的基本反应类型是 ;②据此可知化学反应前后 不变;
③已知“O”的相对原子质量是“●”的 m 倍。该反应中生成物 与
与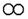 的质量比为 。
的质量比为 。
(1)①2N2 ②O ③ ④3SO42- ⑤He ⑥H2O2
④3SO42- ⑤He ⑥H2O2
(2)①2FeCl3+Cu==CuCl2+2FeCl2 Fe、Cu FeCl3
②Zn、Fe、Cu ZnCl2 因为复分解反应中没有元素化合价变化
(3)分解反应 原子的种类、个数 (m+2)∶m
题目分析:(1)①表示分子个数,在化学式前面加数字,故两个氮分子:2N2 ;②人体中含量最多的常量元素是氧元素,符号为:O;③化合价的表示方法:在元素符号正上方标出化合价。符号在前,数字在后,故+2价的镁元素表示为: ;④离子符号表示方法:在元素符号右上角标明电性和电荷数,数字在前,符号在后,表示离子个数,直接在离子符号前面加数字。故三个硫酸根离子表示为:3SO42-⑤氦气属于稀有气体单质,化学式直接用元素符号表示:He ;⑥氧元素质量分数最高的氧化物过氧化氢,化学式为:H2O2
;④离子符号表示方法:在元素符号右上角标明电性和电荷数,数字在前,符号在后,表示离子个数,直接在离子符号前面加数字。故三个硫酸根离子表示为:3SO42-⑤氦气属于稀有气体单质,化学式直接用元素符号表示:He ;⑥氧元素质量分数最高的氧化物过氧化氢,化学式为:H2O2
(2) ①氯化铁溶液能和单质铜反应生成氯化铜和另一种铁的氯化物。该反应的化学方程式可表示为:2FeCl3+Cu==CuCl2+2FeCl2,根据化合价的一般规律,该反应中,Fe和Cu元素的化合价发生了变化,在反应前后元素的化合价降低,通常具有氧化性,故反应物中表现出氧化性的物质是FeCl3;②向上述反应后的溶液中加入过量的锌粉充分反应后过滤,由于锌的活动性比,Fe和Cu都强,故锌能将Fe和Cu都置换出来,故滤纸上一定有的固体是Zn、Fe、Cu,滤液中的溶质自然只有ZnCl2,在化学反应中,物质所含元素的化合价发生变化的反应就是氧化还原反应,而复分解反应中没有元素化合价变化,故复分解反应一定不是氧化还原反应
(3) ①从反应的微观图可看出,该反应是由一种物质生成两种物质的反应,属于分解反应,②根据质量守恒定律,可知化学反应前后原子的种类、个数不变,
③根据反应的微观图可看出,该反应中生成物 与
与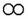 的微粒个数比是2:1,结合“O”的相对原子质量是“●”的 m 倍,故生成物
的微粒个数比是2:1,结合“O”的相对原子质量是“●”的 m 倍,故生成物 与
与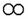 的质量比=(4+2m):2m=(m+2)∶m
的质量比=(4+2m):2m=(m+2)∶m
