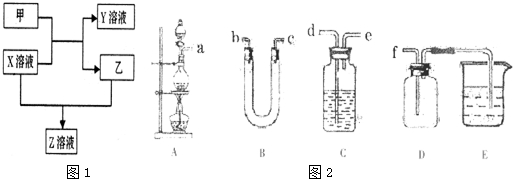
甲、乙是同主族非金属元素组成的单质,乙通常状况下是深红棕色液体.X、Y、Z是化合物.X溶液呈淡绿色,Y、Z的溶液都能使KSCN溶液变红.它们之间有如图1所示转化关系.
请回答:
(1)将Y的饱和溶液滴入沸水中,继续加热可得红褐色液体,此液体不具有的性质是______
A.光束通过该液体时形成光亮的“通路”
B.插入电极通过直流电后,有一极附近液体颜色加深
C.向该液体中加入硝酸银溶液,无沉淀产生
D.将该液体加热蒸干、灼烧后,有氧化物生成
(2)①单质甲、乙和Y溶液中的阳离子氧化性由强到弱的顺序为:______(用化学式表示)
②少量单质甲通入X溶液中发生的离子方程式为______.
(3)实验室制备、收集纯净干燥的甲单质,所需仪器如图2,装置A为发生装置;除装置A中所需的药品外,其他装置中供选择的药品有:浓硫酸、碱石灰、五氧化二磷、饱和食盐水、氢氧化钠溶液.
①装置A中发生反应的化学反应方程式:______.
②按气流的方向连接各仪器接口,顺序为a→______→______→______→______→f.
③指出装置B、C、E中的药品(从提供的药品中选择):
B:______ C:______ E:______.
乙通常状况下是深红棕色液体,应为Br2,甲、乙是同主族非金属元素组成的单质,甲可置换出乙,甲为Cl2,Y、Z的溶液都能使KSCN溶液变红,应含有Fe3+,则X为FeBr2,Y为FeCl3,
(1)将Y的饱和溶液滴入沸水中,继续加热可得红褐色液体,可得到Fe(OH)3胶体,具有丁达尔效应、电泳、聚沉等西行至,将液体加热蒸干、灼烧后,可得Fe2O3固体,加入硝酸银电解质后胶体发生聚沉现象,故答案为:C;
(2)①题中发生反应有Cl2+2Fe2+=2Cl-+2Fe3+,氧化性Cl2>Fe3+,Cl2+2Br-=2Cl-+Br2,氧化性Cl2>Br2,Br2+2Fe2+=2Fe3++2Br-,氧化性Br2>Fe3+,则有氧化性Cl2>Br2>Fe3+,
故答案为:Cl2>Br2>Fe3+;
②由于还原性Fe2+>Br-,少量单质甲通入X溶液中发生反应为Cl2+2Fe2+=2Cl-+2Fe3+,故答案为:Cl2+2Fe2+=2Cl-+2Fe3+;
(3)①实验室用浓盐酸和二氧化锰在加热条件下反应制备氯气,方程式为MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O, △ .
故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O; △ .
②生成氯气中含有HCl、H2O等杂质,先将气体通入饱和食盐水除去HCl,然后通过盛有五氧化二磷的U形管除去H2O,用向上排空法收集,最后用NaOH溶液吸收尾气,
故答案为:a→d→e→b或(c )→c或(b)→f;
③由以上分析可知,B、C、E中的药品分别是五氧化二磷、饱和食盐水、氢氧化钠溶液,
故答案为:五氧化二磷;饱和食盐水;氢氧化钠溶液.

