如图是电解水的简易装置,试回答下列问题.
①与试管a中的电极相连接的是电源的______极(填“正极”或“负极”),试管a中收集到的气体是______,试管a、b中收集到的气体的体积比约为______,
该实验说明水是由______组成的纯净物,说明在化学反应中分子______,而原子______.
②水的摩尔质量为______,水分子中氢、氧原子的物质的量之比为______.
③列出水中氢元素质量分数的计算式.
④3.01×1024个水分子的物质的量是______mol.36g水的物质的量是______mol,含______个氧原子.
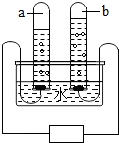
①试管a中产生的气体较多,是氢气,与之相连的是电源的负极;
试管b中产生的气体是氧气,氢气和氧气的体积比约为2:1;
该实验说明水是由氢元素和氧元素组成的;
电解水的过程中,水分子分解成氢原子和氧原子,氢原子之间结合成氢分子,氧原子之间结合成氧分子,说明化学变化中,分子可分,原子不可分.
故填:负;氢气;2:1;氢元素和氧元素;可分;不可分.
②水的化学式是H2O,相对分子质量为:1×2+16×1=18,所以水的摩尔质量是18g/mol;
水分子中氢、氧原子的个数比是2:1,则水分子中氢、氧原子的物质的量之比为2:1.
故填:18g/mol;2:1.
③水中氢元素质量分数的计算式为:
×100%.1×2 1×2+16×1
④1mol水分子的个数为:6.02×1023,3.01×1024个水分子的物质的量为:3.01×1024÷6.02×1023=5mol;
36g水的物质的量为:
=2mol;36g 18g/mol
36g水中氧原子的个数为:6.02×1023×2=1.204×1024;
故填:5;2;1.204×1024.
