⑴生物甲烷是由植物和动物粪便在一定条件下发酵而得的甲烷:

若某植物纤维素的含量为10%,某沼气池,当加入该植物162kg,在微生物作用下完全转化可得CH4在标准状况下的体积为 m3。
⑵合成二甲醚主要步骤为造气和合成。过程如下:
 |
若造气时,设每步转化率均为100%,设某天然气中只含5%CO2,不含其他杂质,每100m3天然气,应同时通入水蒸气和空气各多少体积(空气只含N2和O2,且体积比为4:1,下同),才能保证合成时CO和H2充分利用。V[H2O(g)]= m3;V[空气]= m3。
⑶为了充分利用反应过程中生成的比较纯净的氮气,某企业用天然气为主要原料联合生产二甲醚和氨,过程如下:
制气设备:①CH4+H2O → CO+3H2 ②2CH4+O2 → 2CO+4H2
合成塔Ⅰ:CO+2H2 → CH3OH ; 2CH3OH → CH3OCH3+H2O
合成塔Ⅱ:N2+3H2==2NH3
假设天然气中只含CH4,反应②中通入适量空气,调节①和②投入的CH4的量,以使反应①剩余的H2和反应②剩余的N2的体积比恰好为3:1,以便合成氨。该企业每生产34t NH3理论上同时可以得到二甲醚多少吨?(设工业多次转化,总转化率假定为100%设合成塔Ⅰ中水与CO不反应)?
(1)6.72m3 (2分) (2)10m3,200m3 (每空2分) (3)80.5t (4分)
本题考查多步反应的化学计算,关系复杂,难度较大,容易出错,是一道考查综合思维能力、区分度好的试题。(1)(C6H10O5) n ~ 3nCH4,即C6H10O5 ~ 3CH4
n(CH4)=3n(C6H10O5) =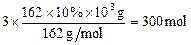
V(CH4)=300mol×22.4L/mol=6.72×103L=6.72m3
(2)依题意,100m3天然气含CH495m3、CO25m3。观察合成反应,CO:H2=1:2时才能充分利用。再观察造气反应,反应(1)必须是(2)的2倍才能达到上述要求。又知反应(2)耗CH4为5m3,则反应(1)耗CH4为10m3,同时需水10m3;所以反应(3)的CH4为80m3,需O240m3,即空气200m3。
(3)由反应N2+3H2==2NH3可求得生产34t氨需1×106molN2和3×106molH2,则反应②通入的O2为1×1/4=0.25×106mol,生成H21×106mol;则反应①应生成H29×106mol,其中用于合成CH3OCH3的H2为6×106mol,由关系式4H2 ~ CH3OCH3可求得:n(CH3OCH3)=(1×106+6×106)mol×1/4=1.75×106mol,为80.5t。
