[江苏省南通中学2008学年度第一学期期末复习高三化学 ].某化学课外活动小组研究乙醇氧化的实验并验证其产物,设计了甲、乙、丙三套装置(图中的夹持仪器均未画出,“△”表示酒精灯热源),每套装置又可划分为①、②、③三部分。仪器中盛放的试剂为:a-无水乙醇(沸点:78 ℃);b-铜丝;c-无水硫酸铜;d-新制氢氧化铜悬浊液。
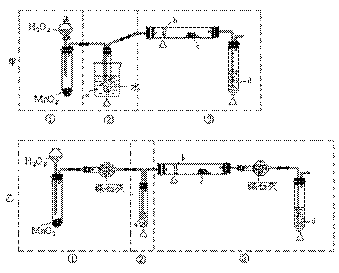
(1)简述两套方案各自的优点:甲:_________________、_________________________,
乙:___________________
(2)集中两套方案的优点,组成一套比较合理完善的实验装置,可按气流由左至右的顺序表示为________________(例如甲①,乙②)
(3)若要保证此实验有较高的效率,还需补充的仪器有__________。理由______。
(4)实验中能验证乙醇氧化产物的实验现象是_______________。
(5)装置中,若撤去第①部分,其它操作不变,则无水硫酸铜无明显变化,其余现象与(4)相同,推断燃烧管中主要反应的化学方程式____________。
(1)甲: ①中用分液漏斗可以控制液体的流量,控制反应的进行;
②中用热水浴加热,可形成较平稳的乙醇气流,使反应更充分;
②中的斜、长导管起到冷凝回流乙醇蒸汽的作用 (三点中答出两点即可,2分)
乙:①与③中的干燥管可防止溶液中的水与无水硫酸铜反应,避免干扰生成物的验证
(2分)
(2)乙①;甲②;乙③ (3分)
(3)温度计(2分);控制水浴温度在78 ℃或略高于78 ℃,使乙醇蒸汽平稳流出,减少挥发,提高反应效率 (2分)
(4)c处无水硫酸铜变蓝;d处生成红色沉淀 (2分)
(5)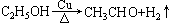 (2分)
(2分)
根据实验目的和两套试验装置的比较可以获得结论。