分某同学为探究铜跟浓硫酸的反应情况,用下图所示装置进行了有关实验
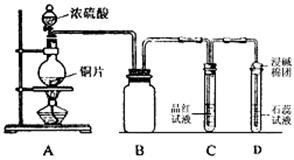
(1)B是用来收集实验中生成的气体的装置,但未将导管画全,请在答题卷上把导管补充
完整 。
(2)请写出铜跟浓硫酸反应的化学方程式 。
(3)实验中D中的现象 。
(4)实验中,该同学取6.4g铜片和12mL 18mol·L-1H2SO4溶液放在圆底烧瓶中共热,直到反应停止,最后发现烧瓶中还有铜片剩余;该同学根据所学的化学知识判断还会有一定量H2SO4的剩余,下列药品中能够用来验证反应停止后的烧瓶中确有剩余的H2SO4的是 填字母编号)。
a.BaCl2溶液 b.Ba(NO3)2溶液 c.银粉 d.Na2CO3粉末
(5)若将16g铜与50mLH2SO4物质的量浓度为一定值的浓硫酸反应,铜完全溶解。请回答:
①反应中产生的气体在标准状况下的体积为 L。
②该反应中被还原的H2SO4的物质的量为 mol。
③待产生的气体全部释放后,向溶液中滴加VmL a mol·L-1NaOH溶液,恰好使溶液中
的Cu2+全部转化为沉淀,则原浓硫酸中H2SO4的物质的量浓度= mol·L-1。
(1)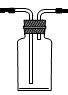 (2)
(2)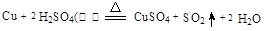
(3)紫色石蕊试液变红 (4)bd (5)① 5.6;② 0.25;③(aV×10-2+5)
题目分析:(1)作图时B装置中导气管长进短出;(2)铜与浓硫酸反应生成二氧化硫和硫酸铜,注意配平;(3)二氧化硫溶于水,得到的的溶液显酸性 ,紫色石蕊试液变红;(4)能够用来验证反应停止后的烧瓶中确有剩余的H2SO4的是b、d,a.反应后生成的硫酸铜中也含有硫酸根离子,能与BaCl2溶液生成白色沉淀,不能检验出硫酸的存在;b.如果溶液中有硫酸剩余,加入Ba(NO3)2溶液,除了生成白色硫酸钡沉淀,还会在烧瓶口处观察到红棕色的NO2气体,故能检验出硫酸的存在;c.加入银粉没有明显变化,不能检验出硫酸的存在;d.如果溶液中有硫酸剩余,加入Na2CO3粉末会生成无色的CO2气体,故能检验出硫酸的存在;(5)①根据铜的质量,利用铜与硫酸反应的化学方程式计算;②根据元素守恒,被还原的H2SO4的物质的量等于生成SO2的物质的量;③“恰好使溶液中的Cu2+全部转化为沉淀”,则此时,溶液为Na2SO4溶液,根据硫元素守恒,则硫酸的物质的量:n(H2SO4)=n(Na2SO4)+n(SO2)=n(NaOH)×1/2+n(SO2),然后根据c=n/V(aq)计算。
