(10分)化学小组同学依据化学反应Zn+2H2SO4(浓) ZnSO4+SO2↑+2H2O制取22.4 L(标准状况)SO2气体。取65.0 g锌粒与98%的浓H2SO4(ρ=1.84 g·cm-3)110 mL充分反应,锌全部溶解。对于制得的气体,有同学认为可能混有氢气。为此,化学小组的同学设计了如下实验装置,对所制取的气体进行探究。
ZnSO4+SO2↑+2H2O制取22.4 L(标准状况)SO2气体。取65.0 g锌粒与98%的浓H2SO4(ρ=1.84 g·cm-3)110 mL充分反应,锌全部溶解。对于制得的气体,有同学认为可能混有氢气。为此,化学小组的同学设计了如下实验装置,对所制取的气体进行探究。

请回答下列问题:
(1)装置A中添加液体的仪器名称为 ;98%的浓H2SO4(ρ=1.84 g/cm3)的物质的量浓度是 ;
(2)请写出产生氢气的反应的离子方程式 ;
(3)①装置B是为了吸收SO2,则不能选用下列试剂中的 (填序号);
A.NaOH溶液 B.浓H2SO4 C.KMnO4溶液
②可证实一定量的锌粒和一定量的浓硫酸反应后生成的气体中混有氢气的实验现象是 ;
(1)分液漏斗 18.4 mol/L (2)Zn+2H+===Zn2++H2↑
(3)① B ②装置E中黑色粉末变红色,F中无水硫酸铜变蓝色 (每空2分)
题目分析:⑴该仪器名称是分液漏斗,C(H2SO4)=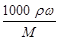 =
=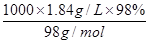 =18.4 mol/L;
=18.4 mol/L;
⑵锌和稀硫酸反应生成硫酸锌和氢气,其离子方程式为Zn+2H+═Zn2++H2↑;
⑶①二氧化硫属于酸性氧化物,能被碱液吸收;具有还原性,能被强氧化性溶液吸收,氢氧化钠溶液呈碱性,高锰酸钾溶液具有强氧化性,即可以用氢氧化钠溶液和高锰酸钾溶液吸收二氧化硫,故选B;
②氢气具有还原性,能将黑色的CuO还原为红色的Cu,且生成水,水能使无水硫酸铜变蓝色,如果有氢气,看到的现象是:装置E中黑色粉末变红色,F中无水硫酸铜变蓝色。
