实验一、定性探究:
①在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,有少量气泡产生,溶液浅黄绿色褪去;
②过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强;
③为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
将第三份加热,看到溶液变浑浊且有大量无色气体产生.
经检测,上述实验中产生的无色气体均为CO2.请回答:
(1)试解释可以在饱和氯水中加入石灰石制备HClO的原因______.
(2)写出步骤③中第一份及第二份滤液发生反应的离子方程式:
第一份:______.
第二份:______.
(3)试根据所学知识推测,在②的滤液中含 有的溶质,除了溶解的极少量氯气外,还含有的其它溶质为(写化学式)______.
实验二、定量探究:
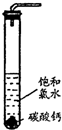
在圆底烧瓶底部,有一用塑料网包住的过量块状碳酸钙和150mL饱和氯水,按如右图所示装置(部分夹持、支撑仪器没有画出)实验,待不再产生气泡后,将塑料网中剩余的石灰石提出液面,密封后再加热、煮沸烧瓶中的液体,直到量筒中的气体不再增加.请回答:
(4)为减少用装置Ⅲ收集气体过程中CO2因溶解而造成的损失,水槽中的水应换为______.
A.饱和碳酸钠溶液 B.饱和碳酸氢钠溶液 C.饱和食盐水
(5)用改进后的装置进行上述实验,测得塑料网内的碳酸钙质量减少Ag,总共收集到标准状况下的CO2气体BL,发现
明显小于BL 22.4L/mol
.若不考虑实验操作和CO2的溶解等因素造成的误差,从化学反应原理来看,导致这一大小关系的原因是______.Ag 100g/mol

(1)在饱和氯水中存在如下平衡:Cl2+H2O

HClO+HCl,盐酸的酸性比碳酸强,而HClO的酸性比碳酸弱,加入过量的CaCO3与溶液中的HCl发生反应,使盐酸的浓度减小,平衡向正反应方向移动,最终生成HClO,
故答案为:在饱和氯水中存在如下平衡:Cl2+H2O

HClO+HCl,加入过量的CaCO3与溶液中的HCl发生反应,使盐酸的浓度减小,平衡向正反应方向移动,最终生成HClO;
(2)加入过量的块状碳酸钙,过量的CaCO3与溶液中的HCl发生反应,最终生成HClO,同时生成Ca(HCO3)2和CaCl2,
所以与石灰水混合,立即产生大量白色沉淀,反应的离子方程式为Ca2++HCO3-+OH-=CaC03↓+H2O,溶液中存在大量的HCO3-离子,加入盐酸,发生HCO3-+H+=CO2↑+H2O,会有大量气体生成,
故答案为:Ca2++HCO3-+OH-=CaC03↓+H2O;HCO3-+H+=CO2↑+H2O;
(3)由实验③可知,除HClO外,还生成Ca(HCO3)2和CaCl2,故答案为:HClO、Ca(HCO3)2、CaCl2;
(4)二氧化碳难溶于饱和碳酸氢钠溶液,可用排饱和碳酸氢钠溶液的方法收集二氧化碳气体,故答案为:B;
(5)碳酸氢钙不稳定,加热生成碳酸钙和二氧化碳,导致生成的二氧化碳的物质的量小于原碳酸钙的物质的量,
故答案为:碳酸钙与氯水反应生成的 Ca(HC03)2 再受热时,除生成 CO2 外,还生成了 CaC03.
