(10分)FeCl3溶液中,加入难溶于水的CaCO3粉末,观察到CaCO3逐渐溶解,产生无色气体和红褐色沉淀。则:
(1)气体为 ,红褐色沉淀为
(2)上述现象产生的理由是(用离子方程式及简要文字表
在Na2CO3溶液中滴加酚酞显红色。
(3)溶液显红色的原因是(写离子方程式)
(4)将溶液加热观察到的现象为
(5)在溶液中加足量BaCl2溶液,观察到的现象为
(10分)(1)CO2、Fe(OH)3
(2)Fe3++3H2O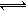 Fe(OH)3+3H+ CaCO3+2H+=Ca2++ H2O+CO2↑,促进Fe3+水解生成Fe(OH)3沉淀。
Fe(OH)3+3H+ CaCO3+2H+=Ca2++ H2O+CO2↑,促进Fe3+水解生成Fe(OH)3沉淀。
(3) CO32—+H2O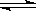 HCO3—+OH—
HCO3—+OH—
(4)红色加深
(5)红色褪去且产生白色沉淀
考查盐的水解及水解平衡的移动
(1)、(2)FeCl3易水解,溶液呈酸性:Fe3++3H2O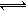 Fe(OH)3+3H+,加入CaCO3后:CaCO3+2HCl=CaCl2+H2O+CO2↑,使水解平衡右移,最终生成红褪色Fe(OH)3沉淀
Fe(OH)3+3H+,加入CaCO3后:CaCO3+2HCl=CaCl2+H2O+CO2↑,使水解平衡右移,最终生成红褪色Fe(OH)3沉淀
(3)、(4)、(5):Na2CO3溶液水解呈碱性:CO32—+H2O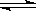 HCO3—+OH—,加入酚酞,溶液呈红色;
HCO3—+OH—,加入酚酞,溶液呈红色;
由于水解平衡正反应为吸热反应,加热促进平衡右移,碱性增强,红色加深
加入BaCl2溶液:CO32-+Ba2+=BaCO3↓,CO32-浓度减小,平衡左移,碱性减弱,故红色褪去且产生白色沉淀
